“如果用一句話形容我目前的科研工作,那就是利用酵母細胞工廠高效製造高附加值生物產品。” 在接受生輝 SynBio 採訪時,天津科技大學生物工程學院於愛群教授總結道。
作為合成生物學領域最為典型的應用 —— 細胞工廠,是透過對微生物進行特殊改造,引入定製的生產線來加工製造人們所需要的各種產品,比如食品、藥品、生物燃料等等。
例如,可以用細胞工廠來生產可降解塑膠,從而避免化工合成塑膠對環境造成的汙染;也可以生產檸檬烯等各種單萜化合物,從而大幅縮短其製造週期、降低其製造成本、提高產量……
細胞就好比製造產品的車間,代謝通路是生產線,培養基提供原料和動力,細胞內複雜的反饋和調控機制則是生產管理系統。只有細胞工廠內各個部門之間密切協調配合,才能實現目標產品產量的最大化。
近期,於愛群教授在 Biotechnology Advances、ACS Synthetic Biology、Biotechnology for Biofuels、《微生物學通報》、《食品工業科技》等期刊發表數篇論文,分析和總結了近年來在解脂耶氏酵母以及其他微生物底盤細胞中,利用代謝工程及合成生物學技術構建細胞工廠生物合成一些單萜化合物方面的研究進展,討論了該方法目前所面臨的瓶頸問題及其可能的解決措施,為在微生物細胞工廠中實現單萜化合物的規模化、效益化工業生產提供可能的理論依據。
藉此機會,生輝 SynBio 邀請到了於愛群教授,來與我們分享他的研究成果。
單萜化合物 —— 極具潛力的工業原料
作為廣泛存在於植物中的天然產物,單萜化合物在眾多領域均有著廣泛用途,市場潛力巨大。另外,隨著人們對健康和環境可持續性的日益重視,一些單萜化合物和相關衍生物因其獨特的環境友好特性在各種工業應用中越來越受到青睞,而且很多單萜化合物具有重要的生理活性,是開發新藥和研究天然產物的重要來源。
單萜化合物:
為萜類化合物的一種,是由二分子異戊二烯聚合而成的烯烴類化合物,及其含氧的和飽和程度不等的衍生物。
單萜化合物分為直鏈型、單環型、雙環型以及三環型,廣泛分佈於高等植物的腺體、油室和樹脂道等分泌組織中。單萜含氧衍生物(如醇類、醛類、酮類)具有較強的香氣和生物活性,是食品、飲料、醫藥、化妝品工業的重要原料。
一般來說,傳統獲取單萜化合物的方法有兩種:從天然植物中進行提取、分離和化學合成方法。
但植物生長週期緩慢、資源稀缺,而且植物體內單萜化合物的含量較低,提取和分離工藝要求較高,難以大量獲得,所以難以滿足日益增長的消費和工業需求;化學合成的方法也存在著嚴重依賴化石燃料、能源消耗大、合成反應效率低,以及產生大量有機廢物容易造成環境汙染等缺點。
因此,開發用來生產單萜化合物的可再生微生物資源(來補充甚至代替原有稀少珍貴的植物資源),以及單萜類化合物的低成本高效率、可持續和生態友好的替代生產路線的需求亟待解決。
近年來,隨著合成生物學的發展,代謝工程等相關技術取得了一系列突破性進展,透過對微生物細胞進行特定改造並利用細胞工廠異源合成單萜化合物,將有望成為替代植物提取和化學合成的一種更好的策略。
這種藉助微生物細胞工廠進行生物合成的方法具有成本投入少、環境汙染小、量產規模可控等諸多優點,是建設節約型社會、實現可持續發展的綠色生產方式。不論從生態環保、投產比,亦或是產業規模來看,這種生物合成單萜化合物的方法均具有很大優勢。
解脂耶氏酵母 —— 高效的合成利器
所謂 “工欲善其事必先利其器”,選對 “器具” 很關鍵。如上文所述,採用合成生物學的方法生產單萜化合物很有潛力,具體採用哪種微生物細胞進行合成呢?這裡經常使用的是一種名為解脂耶氏酵母的細胞。
解脂耶氏酵母(Yarrowia lipolytica):
於 1942 年首次被分離得到,為非常規酵母中具代表性的一種,同時也是一種公認安全的微生物。
解脂耶氏酵母有廣泛的底物譜,能利用有機酸(如檸檬酸、異檸檬酸等)、烷烴類廉價物質等作為底物來生產單萜 / 萜類化合物、生物燃料等多種高附加值產物。
自上世紀 40 年代被成功分離以來,解脂耶氏酵母便受到廣大研究者的重視。因其能夠安全地用於食品和藥物生產、具有較好的脂類合成能力、碳源譜廣泛等優點,解脂耶氏酵母常被用作宿主菌來生產各種有用的化合物。目前,解脂耶氏酵母仍然是非常規酵母中使用最為廣泛的底盤細胞之一。
對此,於愛群表示,解脂耶氏酵母是異源合成單萜化合物理想的微生物底盤細胞,近年來利用代謝工程及合成生物學技術在解脂耶氏酵母底盤細胞中重構與最佳化單萜化合物的合成途徑來實現目標代謝產物的高效合成,已經成為一項新的研究熱點。

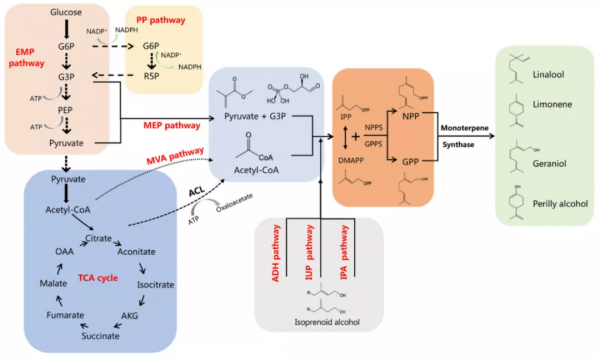
圖|解脂耶氏酵母異源合成單萜及其他萜類化合物的代謝途徑 [2]。
與常規酵母(如釀酒酵母)相比,解脂耶氏酵母具有一系列優勢,可總結為以下五點:
① 自身具有將多種廉價生物質原料快速轉化為各種高附加值化學品如檸檬酸、琥珀酸的代謝能力,生產基於脂質的油性化學品的能力也較強;
② 對油脂類物質具有較強的降解能力,因此可用於對廢油汙染的生物修復;
③ 具有更高效分泌蛋白質和有機酸(如 α- 酮戊二酸和琥珀酸)的能力;
④ 對生長條件的要求更低,在各種碳源、pH 和鹽度條件下均可生長;
⑤ 不受葡萄糖效應的影響,因此不會進行有氧酒精發酵。[2]
與大腸桿菌相比,解脂耶氏酵母具有完整的內膜系統和與植物相類似的蛋白質翻譯後修飾系統,更適合植物源蛋白質的表達。此外,解脂耶氏酵母屬於典型的產油酵母,細胞內脂肪酸(Fatty Acid)、脂醯輔酶 A(Fatty Acyl-CoA)以及乙醯輔酶 A(Acetyl-CoA)的積累量較高,因此,在生產單萜化合物方面具有明顯優勢。
當下,隨著解脂耶氏酵母全基因組序列的公佈以及基因表達載體、遺傳轉化方法、合成生物學元件和基因編輯技術的快速發展,解脂耶氏酵母已經成為目前代謝工程及合成生物學研究中備受關注且極具潛力的底盤細胞之一。
圖|在解脂耶氏酵母中異源生產單萜及萜類化合物示例 [2]。如圖所示,近年來,研究人員藉助代謝工程以及相關合成生物學技術,實現了多種單萜及萜類化合物合成途徑在解脂耶氏酵母底盤細胞中的重構與最佳化。例如,外源引入的橙花基焦磷酸合酶(NDPS1)可催化異戊烯基焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP)轉化生成橙花基焦磷酸(NPP),NPP 作為植物源檸檬烯合酶(LS)的底物進一步轉化為單萜化合物 —— 檸檬烯。[2] (生輝整理)
然而,解脂耶氏酵母也並非十全十美。對此,於愛群指出,由於對解脂耶氏酵母的研究及應用起步較晚,因此目前尚未完全掌握該底盤細胞內的基因表達調控等分子機制,而且遺傳作業系統也有待進一步完善。另外,該酵母固有的一些特性也在一定程度上限制了單萜化合物的產量,距離大規模工業化生產還有很長的路要走。
接下來,需要不斷地對其中的核心機制和關鍵技術進行創新性的探索和研究。未來需要重點突破的四個方面如下:
① 解脂耶氏酵母本身不含有可自主複製的遊離質粒,因此在對其進行基因編輯時需要首先構建人工合成質粒作為過渡載體,較為費時費力;
② 解脂耶氏酵母胞內的非同源重組效率極高,從而導致基因定點敲除和敲入都非常困難。雖然 CRISPR-Cas9 介導的基因整合技術能將酵母同源重組的成功率提高到 50%-70%,但該技術也仍未完全解決其更傾向於進行非同源重組的問題。
③ 解脂耶氏酵母是嚴格需氧的非發酵酵母,只有在氧氣充足時才能實現最佳的生長狀態,這可能是大規模工業發酵生產單萜化合物潛在的制約因素。
④ 當前提高解脂耶氏酵母合成單萜化合物產量的主要方式仍侷限於透過增強途徑關鍵酶基因的表達量來增加前體物質的供應量,未來需要開發出更多適用於解脂耶氏酵母的創新工具和技術。[2]
代謝工程 —— 先進的加工技藝
就像燒菜一樣,有了 “食材” 和 “炊具”,想要做出美味的菜餚,接下來的重點便是 “烹飪”。目前,透過生物合成途徑生產單萜化合物常用的技術手段是 “代謝工程”。
代謝工程(Metabolic engineering):
又稱途徑工程,是利用多基因重組技術有目的的對細胞代謝途徑進行修飾改造以改變細胞特性,並與細胞基因調控、代謝調控及生化工程相結合,最終實現構建新的代謝途徑生產特定目標產物的方法。
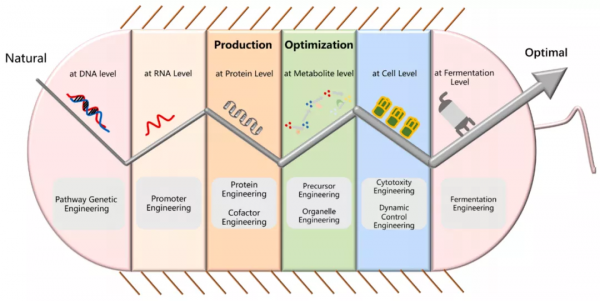
在最新發表的綜述論文中,於愛群對目前利用微生物代謝工程技術生產單萜類化合物的進展進行了全面梳理,全面深入地總結和剖析了上下游各個過程中所用各種策略所存在的優點和侷限性。不同於以往,此次是從最上游到最下游,即在 DNA、RNA、蛋白質、產物、細胞和發酵等不同水平上對已用策略進行了分類分析。
如上圖所示,目前,微生物細胞工廠已經在 DNA 水平、RNA 水平、蛋白質水平、代謝物水平、細胞水平、發酵水平上進行了系統工程改造,透過強大的代謝工程工具高效合成高附加值的單萜化合物。這些代謝工程工具主要包括:途徑基因工程、啟動子工程、輔助因子工程、蛋白質工程、前體工程、細胞器工程、細胞毒性工程、動態控制工程、以及基於方法和技術的發酵工程。[1]
就現階段而言,透過代謝工程技術生產各類單萜化合物的研究主要集中於解脂耶氏酵母、釀酒酵母和大腸桿菌等幾種微生物底盤細胞。
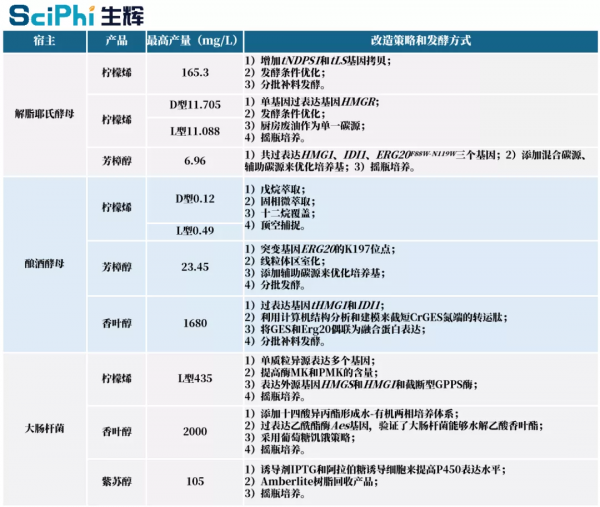
圖|透過代謝工程改造微生物細胞生產單萜化合物的產量及策略 [3](生輝整理)
利用代謝工程構建的細胞工廠為單萜化合物的綠色生產提供了全新的路線。如上圖所示,透過代謝工程對特定微生物細胞的代謝途徑進行改造,最佳化或改變微生物細胞原有的代謝和表達調控網路,現階段已經成功實現了包括檸檬烯、芳樟醇、香葉醇、紫蘇醇等在內的多種單萜化合物的微生物異源合成。[3]
代謝工程中的具體調控方式主要是在轉錄水平、翻譯水平以及蛋白質水平上的調控等。目前的主流思路是透過強化目標產物合成途徑中代謝通量來對微生物底盤細胞進行改造,進而實現目標產物產量的提高。
另外,於愛群也指出了當前利用代謝工程改造微生物細胞生產各類單萜化合物所面臨的一些挑戰,主要歸結為以下兩點:
其一,採用的微生物底盤細胞的不同,對目標產物的終產量有直接影響,而目前的研究還主要侷限在解脂耶氏酵母、釀酒酵母和大腸桿菌等為數不多的底盤細胞中,有待進一步拓展;
其二,依現有技術水平,相關產物在這幾種微生物底盤細胞中的產量基本都是毫克級,現階段還很難滿足產業化生產的實際要求。
於愛群表示,目前大多數研究者是從某一個點切入對單萜合成路徑進行適配和最佳化來提高產物產量,而缺少了對多種代謝工程策略的協作使用,因而難以實現系統性的全域性最佳化,此外,研究者們還往往忽略掉單萜合成之後的儲存、外排及捕獲過程。
為了構建出能夠高效合成單萜化合物的細胞工廠並最終實現綠色製造,需要深入探究影響不同微生物底盤細胞高效生產特定目標產物的關鍵機制及核心問題,還需要進一步明確不同微生物底盤中合成單萜化合物的關鍵控制節點和與之相對應的控制策略。
對於接下來的研究重點,於愛群列舉了應該著力攻關的四個方向:
① 底盤細胞。底盤細胞是各種生化反應進行的場所,未來需要發掘新的、更有工業應用前景的非模式微生物底盤細胞,並找到不同產物與底盤細胞之間的最大相容性。另外,利用合成生物學技術構建微生物基因組精簡最佳化的底盤細胞也有望成為提高單萜化合物產量的重要策略。
② 培養基。培養基的成分是決定底盤細胞合成目標物能力高低的重要因素,為了提高目標物產量,未來需要進一步最佳化培養基成分,以及篩選產物合成途徑中相關限速酶啟用劑。
③ 代謝工程策略。只有明確了代謝過程中的關鍵限制因素,才能有的放矢,實現目標產物產量、產率的大幅提高。因此未來需要利用更理性全面的策略和更先進的技術方法,深入探究影響不同微生物底盤高效生產特定目標產物的限速步驟、關鍵機制及核心問題。
④ 代謝產物耐受性。代謝產物的不斷積累可能會對微生物底盤細胞造成毒害。比如單萜化合物會引起微生物細胞壁、細胞膜和細胞器膜等結構的破壞,降低某些酶的活性,阻礙細胞生理活動的正常進行,最終導致微生物死亡。未來可以利用誘變育種或適應性進化等技術篩選出耐受性更強的菌株作為底盤細胞。此外,還可以採用萃取、樹脂吸收或膜過濾等分離技術,及時地把單萜產物從培養環境中分離出來,實現 “邊產生邊分離”。
除了上述四點之外,還可以利用由多種微生物底盤細胞組成的混合發酵系統,以及無細胞表達系統等策略來突破現有的一些限制性因素,從而提高代謝工程設計和改造的效率,這將有助於提高利用微生物細胞工廠合成單萜化合物的生產水平。[3]
“總之,必須做到上下游系統性的全域性最佳化,才能大幅提高產物產量,實現生產成本的下降。當然,這種系統性的全域性最佳化不是一蹴而就的,需要先找到各個過程中的關鍵限制點,然後再抓住關鍵點各個擊破。換句話說就是需要 “由面及點,點面結合”,現在我們正在採取的策略就是這樣的。” 於愛群補充道。
總結與展望
合成生物學是一門綜合了生物學、物理學、計算機學和工程學等眾多學科知識於一體的新興前沿交叉學科,雖然只是生命科學領域中一個新的分支,但合成生物學已經被認為是 21 世紀最重要的生物技術平臺。
合成生物學從概念的提出到具體應用不過短短十餘年的時間,合成生物學理論和技術的迅猛發展對生命科學基礎研究和工業生物技術產生了深遠影響,如今已經在微生物細胞工廠的構建方面獲得了不小成就,其透過生物合成各種高附加值產品的綠色生產方式展現出了巨大的應用前景和賦能潛力。
最近幾年,人工智慧開始爆發,對此,於愛群認為:將合成生物學、人工智慧,還包括計算生物學、生物資訊學等新興的先進技術與傳統的代謝工程進行交叉合作,是今後生物製造領域發展的大勢所趨,有望帶來產業革命,對於單萜化合物的生物合成也不例外。
談及技術產業轉化,於愛群表示,目前已與新加坡國立大學的 Jee Loon Foo、新加坡理工學院的 Adison Wong、廈門大學的袁吉鋒、中山大學的巫瑞波等團隊建立了密切的合作關係,正在共同推動幾種高附加值產品的產業化。
關於合成生物學對傳統發酵工業的作用,於愛群指出:目前的生物發酵過程還存在效率低、機制不明確等問題,未來如何將先進的合成生物學技術與方法合理地運用到生物發酵過程中,並進行完美融合,起到最大的正向作用,將是未來研究的方向。
於愛群總結歸納了接下來需要努力的幾個方面:
第一,需要有豐富的理論知識積累。包括生物化學、發酵工程、微生物學、基因工程等方面的基礎知識都要掌握;
第二,需要不斷學習、與時俱進。合成生物學的發展很快,每天都有大量文章、理論、技術、資訊的更新;
第三,設計實驗是一回事,更重要的是多做實驗。生物屬於實驗科學,絕大部分結果都是需要實驗才能取得的,所以那種合成生物學技術和方法有沒有用,不是想出來的,必須要進行實驗驗證。
採訪接近尾聲,於愛群概括道:“合成生物學具有定向、快速、高效、準確、可控、高通量、智慧化、自動化、高效化等許多優點,這些都是傳統的生物發酵工業所比較缺少的東西。所以,合成生物學能夠成為促進構建高效生物發酵工業的新引擎與新動力。我相信,合成生物學的發展會給生物發酵工業帶來深刻變革,甚至是帶來新一輪的產業革命。”