第一作者:HanweiZhou
通訊作者:Kyle R.Crompton、Partha P.Mukherjee
通訊單位:美國普渡大學、美國海軍水面作戰中心克蘭分部
【研究背景】
儘管新興的高效能電極材料如富鎳層狀過渡金屬氧化物正極和鋰金屬/矽石墨複合負極極大地提升了鋰離子電池的比能量,但其仍然受到安全性的限制。在機械、電或熱濫用的情況下,鋰離子電池可能會經歷過度的溫升併發生災難性的熱失控(TR)。預測鋰離子電池熱安全事件的發生對於最佳化具有高耐熱性的電化學體系具有重要意義。儘管許多文獻已經研究了單個電池材料的熱釋放,但在熱濫用情況下電極間化學串擾的安全危害仍然沒有受到較大的關注,因此需要一個基本的瞭解。
圖 1、鋰離子電池的熱安全事件。
【工作簡介】
近日, 美國普渡大學的Partha P.Mukherjee和海軍水面作戰中心克蘭分部的Kyle R.Crompton等人使用差示掃描量熱法(DSC),輔以全電池加速量熱法(ARC)和計算模型,對從商用鋰離子電池中收集的各種材料樣品進行綜合熱分析,並描繪了電解質、溼正極、溼負極和模擬電池分層結構的DSC全電池樣品的反應動力學,以揭示電極之間大量的熱相互作用。利用Kissinger方法和機理驅動的非線性最佳化策略,估計了反應機理的高解析度動力學引數。基於所提取的動力學引數建立了熱濫用模型,模擬了電池層級熱失控現象,並與實驗觀測結果進行了比較,表明層間串擾效應對鋰離子電池化學結構熱安全特性的顯著影響。相關研究成果以“Effect of Electrode Crosstalk on Heat Release in Lithium-ion Batteries under Thermal Abuse Scenarios”為題發表在國際頂尖期刊Energy Storage Materials上。
【內容詳情】
電池效能和電極特性
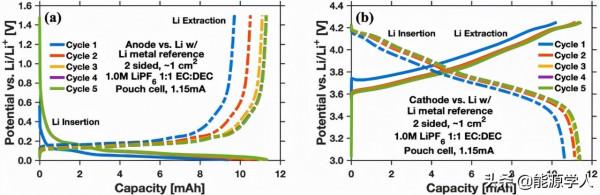
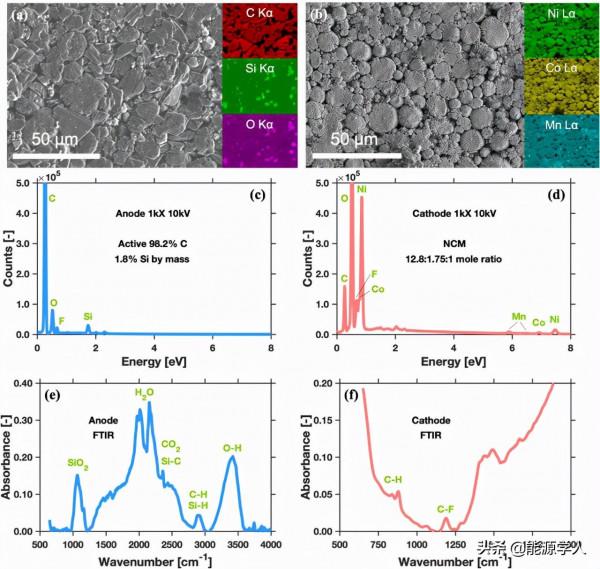
圖2(a-b)顯示,五個迴圈後,回收後的負極和正極電池容量分別穩定在11.3mAh和11.4mAh。圖3(a-d)顯示,負極樣品的組成為摻矽石墨,正極樣品的組成為鋰鎳鈷錳氧化物。圖3(e-f)顯示,負極粘結劑由羧甲基纖維素(CMC)和丁苯橡膠(SBR)組成,而正極中存在聚偏二氟乙烯(PVDF)粘結劑。
圖 2、具有(a)回收石墨負極和(b)回收NCM正極的迴圈效能。
圖 3、(a)石墨負極和(b)NCM正極的SEM和EDS。(c)石墨負極和(d)NCM正極的EDS計數訊號和能量色散。(e)石墨負極和(f)NCM正極的FTIR光譜。
電解質熱特徵的動力學分析
電解質樣品的DSC曲線如圖4(a)所示,掃速為3、5、7和9℃/min。在200℃之前沒有觀察到明顯的熱反應。從200℃開始,電解質樣品顯示出一個吸熱反應,然後在測試結束前出現兩個放熱反應。
圖 4、(a)電解質的DSC曲線,掃速為3、5、7和9℃/min。(b)關於電解質放熱反應峰的Kissinger方法。(c)電解質在相應DSC曲線上的非線性最佳化。
利用Kissinger方法對DEC和EC峰資料進行線性擬合,決定係數(R2)為0.9663和0.9997。在3℃/min到9℃/min下對DSC曲線進行非線性最佳化。基於Arrhenius方程的建模結果如圖4(c)所示,R2為0.9551、0.9819、0.9416和0.9406。
溼正極熱特徵的動力學分析
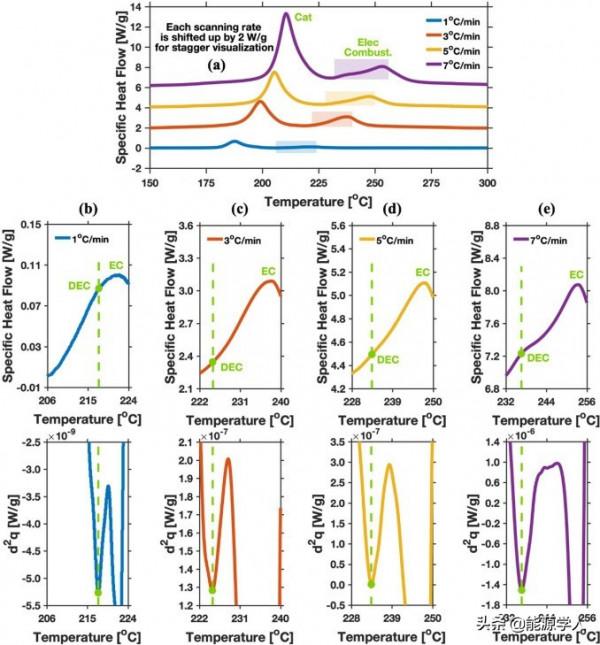
溼正極樣品的DSC曲線如圖5(a)所示,掃速為1、3、5和7℃/min,對應的第一放熱反應的峰值溫度分別為187.7℃、199.2℃、205.4℃和210.5℃。第一個反應峰歸因於高鎳NCM正極中活性材料的分解。
圖 5、(a)溼正極的DSC曲線。在(b) 1℃/min,(c) 3℃/min,(d) 5℃/min,(e) 7℃/min情況下,DEC和EC燃燒反應的區域性放大檢視以及相應的比熱流二階差分(d2q)。
NCM正極的主要副反應是氧釋放。因此,由於正極分解產物的強氧化作用,第二個反應峰歸因於電解質燃燒。圖5(b-e)顯示了電解質燃燒區的區域性放大圖,以及相應的比熱流二階差分(d2q)。在所有四個d2q圖中都可以觀察到兩個區域性最小值點,表明兩個反應峰部分合並。第一次放熱反應的峰值溫度分別為217.4℃、224.9℃、233.4℃和236.6℃。第二個放熱反應的峰值溫度分別為221.9℃、237.9℃、247.7℃和253.4℃。第一個峰對應DEC燃燒,第二個峰對應EC燃燒。
圖6(a)顯示,利用Kissinger方法對正極分解、DEC燃燒和EC燃燒峰值溫度的線性擬合表明,其R2分別為0.9974、0.9621和0.9960。在所有四個DSC實驗曲線上都實施了非線性最佳化。模擬結果如圖6(b)所示,在1℃/min到7℃/min下,R2分別為0.9592、0.9871、0.9747和0.9626。
圖 6、(a)溼正極放熱反應峰的基辛格方法。(b)溼正極在相應DSC曲線上的非線性最佳化。
溼負極熱特徵的動力學分析
圖7(a)為溼負極樣品的DSC曲線,掃速為3、5、7和9℃/min,第一放熱反應的峰值溫度分別為113.5℃、117.0℃、124.5℃和126.5℃。它歸於石墨負極表面SEI層的分解,區域性放大區如圖7(b)所示。
圖 7、(a)溼負極的DSC曲線。(b) SEI分解反應的區域性放大檢視。在(c)3℃/min,(d) 5℃/min,(e) 7℃/min,(f)9℃/min情況下,負極-粘結劑和負極-矽反應的區域性放大檢視。
第二個放熱反應的峰值溫度分別為250.5℃、267.5℃、274.3℃和279.4℃。第三個放熱反應的峰值溫度分別為265.9℃、285.0℃、295.6℃和301.0℃。它們對應DEC和EC的分解反應。第四個放熱反應的峰值溫度分別為286.3℃、314.3℃、318.8℃和321.3℃。第五個放熱反應的峰值溫度分別為289.2℃、318.2℃、338.1℃和339.9℃。圖7(c-f)顯示了它們的區域性放大圖。第四個放熱反應歸因於石墨負極和CMC/SBR粘結劑之間的熱相互作用。由於在石墨負極中檢測到1.8 wt%的矽相。因此,第五個放熱反應歸因於石墨負極和矽奈米顆粒之間的熱相互作用。第六個放熱反應的峰值溫度分別為308.4℃、328.5℃、355.6℃和372.8℃。這是由於原始SEI層、CMC/SBR粘結劑和矽奈米顆粒的保護失效,暴露的插層鋰與電解質之間的熱相互作用造成。
利用Kissinger方法對SEI 膜分解、DEC分解、EC分解、負極-粘結劑相互作用、負極-矽相互作用和負極-電解質相互作用的峰值資料擬合結果如圖8(a)所示,其中R2的值分別為0.9370、0.9734、0.9832 、0.8425、0.9408和0.9688。對每個掃速的建模結果進行非線性最佳化,如圖8(b)所示。圖8(c)顯示了SEI分解區的放大圖。從3℃/min到9℃/min,R2的值分別為0.5956、0.8575、0.9040和0.9340,表明在3℃/min和5℃/min的情況下擬合度不足。
圖 8、(a)溼負極放熱反應峰的基辛格方法。(b)溼負極在相應DSC曲線上的非線性最佳化。(c)SEI分解反應非線性最佳化的區域性放大檢視。
DSC-全電池熱特徵的動力學分析
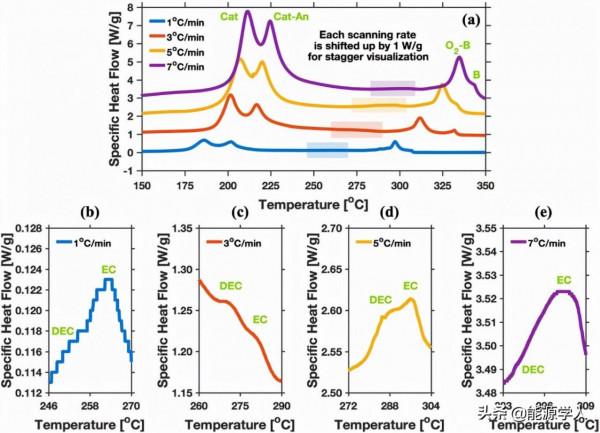
全電池樣品的DSC曲線如圖9(a)所示,掃速為1、3、5和7℃/min。透過仔細檢查可以確定四個明顯的放熱反應和兩個微弱的放熱反應。第一次放熱反應的峰值溫度分別為186.1℃、201.6℃、207.1℃和211.5℃。第二個放熱反應的峰值溫度分別為201.8℃、216.8℃、219.9℃和224.6℃。析氧為正極分解過程中的主要副反應,因此第二個放熱反應被歸為由析氧引起的正極和負極之間的化學串擾。
圖 9、(a)DSC全電池的DSC曲線。在(c)1℃/min,(d) 3℃/min,(e)5℃/min,(f)7℃/min情況下,DEC和EC分解反應的區域性放大檢視。
隨著溫度的進一步升高,出現不太明顯的第三和第四放熱反應。第三個放熱反應的峰值溫度分別為255.9℃、273.0℃、285.2℃和287.4℃。第四個放熱反應的峰值溫度分別為263.5℃、282.0℃、296.2℃和302.0℃。圖9(b-e)顯示了其放大區。這兩個反應可歸因於少量DEC和EC殘留物的分解。第五個放熱反應的峰值溫度分別為297.4℃、311.9℃、324.8℃和334.8℃。它歸因於釋放的氧和電極粘結劑之間的熱相互作用。第六個放熱反應的峰值溫度分別為306.8℃、331.9℃、333.5℃和343.6℃。它對應在第五次氧-粘結劑相互作用後剩餘的CMC/SBR和PVDF粘結劑的脫氫和脫氟化氫反應。
利用Kissinger方法對正極分解、正極-負極串擾、DEC殘留分解、EC殘留分解、氧-粘結劑相互作用和粘結劑殘留分解的峰值資料擬合結果如圖10(a)所示,其中R2分別為0.9954、0.9810 、0.9857、0.9903、0.9639和0.9513。圖10(b)顯示了對四種掃速進行非線性最佳化的模擬結果。DEC和EC殘留分解的放大圖分別顯示在圖10(c)中。從1℃/min到7℃/min,R2的值分別等於0.9632、0.9821、0.9873和0.9885。
圖 10、(a) DSC-全電池放熱反應峰的基辛格方法。(b)DSC-全電池在相應DSC曲線上的非線性最佳化。(c)DEC和EC分解反應非線性最佳化的區域性放大檢視。
串擾對電池級TR特性的影響
圖11(a)顯示,串擾模型無法預測自加熱過程的開始,因為DSC全電池樣品的DSC曲線和隨後的動力學分析沒有量化150℃之前的放熱反應。然而,串擾模型很好地預測了198.7℃和1060分鐘的TR。
圖 11、(a)基於3.6Ah商用18650鋰離子電池的ARC串擾模型和ARC實驗的溫度曲線。(b)ARC串擾模型和ARC實驗的升溫速率以及串擾模型中涉及的每個放熱反應的發熱速率及其總量。
圖11(b)顯示,串擾模型的升溫速率顯示,兩個峰值溫度分別為346.3℃和470.1℃,與實驗曲線上的兩個平臺基本匹配。正極分解和正極-負極串擾對應198.7℃和375.4℃之間的第一個凸起,而氧-粘結劑相互作用和粘結劑分解對應375.4℃和566.2℃之間的第二個小凸起。
圖12(a)顯示,隔離模型的自加熱過程開始於82.0℃和272分鐘,與實驗資料有5.0℃的溫度差和28分鐘的時間差。隔離模型預測的TR開始為198.7℃和5713分鐘,與198.7℃和1058分鐘的實驗結果存在較大偏差。總體而言,隔離模型顯示出的熱量比串擾模型少。因為其主要涉及以負極為中心的反應,尤其是負極-電解質相互作用。
圖 12、(a)基於3.6Ah商用18650鋰離子電池的ARC隔離模型和ARC實驗的溫度曲線。(b)ARC隔離模型和ARC實驗的升溫速率以及隔離模型中涉及的每個放熱反應的發熱速率及其總量。
圖12(b)顯示,隔離模型的升溫速率在198.7℃和357.1℃之間存在一個凸起,然後在103℃和519.2℃之間出現一個平臺,與實驗曲線匹配。正極分解主導了隔離模型中升溫速率的第一個凸起,而DEC燃燒和釋放的電能起次要作用。而釋放的電能在隔離模型中主導平臺區,其中EC燃燒和EC分解貢獻較小。
【結論】
電解質存在兩個放熱反應,對應於DEC溶劑的分解和EC溶劑的聚合。溼正極存在兩種放熱反應,分別對應NCM正極中活性材料的分解和氧釋放導致的電解質燃燒。溼負極呈現六個放熱反應,依次為SEI分解、DEC和EC分解、石墨負極與CMC/SBR粘結劑之間的相互作用、石墨負極與矽奈米顆粒之間的相互作用以及嵌入鋰與電解質的相互作用。ARC串擾模型可以準確預測TR的開始,但無法捕獲自放熱,而ARC隔離模型能夠準確地預測自放熱的開始但不能預測TR。
HanweiZhou,MukulParmananda,Kyle R.Crompton,Michael P.Hladky,Martin A.Dann,Jason K.Ostanek,Partha P.Mukherjee. Effect of Electrode Crosstalk on Heat Release in Lithium-ion Batteries under Thermal Abuse Scenarios. Energy Storage Materials. 2021, DOI:10.1016/j.ensm.2021.10.030