*僅供醫學專業人士閱讀參考
肺癌以其不斷增長的發病率和死亡率對人們健康和生命造成了極大的威脅。雖然近年來新藥發展迅速,但外科手術仍然是治療肺癌的主要手段。約30%-35%的非小細胞肺癌(NSCLC)患者屬於可手術切除,但IB-III期患者術後2年複發率高達50%以上,對後續的生存和預後造成很大影響,如何提高這部分患者的生存率成為臨床上亟待解決的問題。
輔助治療對晚期NSCLC患者有何價值?
可手術的NSCLC患者在術後達到R0清除後,隱匿性轉移以及一些非區域性的胸腔內轉移仍可能存在,除此之外,遠處轉移也是限制早期肺癌患者生存的重要原因。根據美國癌症聯合委員會第八版分期(AJCC8),IB期NSCLC患者的5年生存率為68%,II期患者為53%-60%,III期患者更可能僅有30%左右,並且大部分的治療失敗還伴隨著復發轉移,因此在術後進行輔助治療對於提高早中期患者的長期治療結果十分重要的。
自2008年LACE薈萃分析結果公佈以來,可手術肺癌患者術後輔助化療便成為了標準治療方案,而在輔助化療帶來的無病生存期(DFS)、總生存期(OS)獲益主要集中於腫瘤>4cm的高危IB期,以及II期和IIIB期可手術患者,而且療效相對有限,僅能將患者的5年生存率提升約5%,聯合放療等區域性治療的探索也大多未實現陽性結果,出現了明顯的療效瓶頸[1],所以靠傳統的治療模式已經很難再有進一步的突破。
EGFR突變是肺癌最常見的基因突變型別,目前的治療方案是EGFR-TKI治療,相比化療時代,靶向治療的提升了晚期肺癌患者的生存時間。隨著近幾年一些關於肺癌術後輔助靶向治療的臨床研究資料更新,輔助靶向治療成為肺癌領域關注的焦點。
術後輔助靶向治療獲益人群篩選成為診療關鍵
術後輔助治療經歷了長時間的探索,從過去的肺癌輔助靶向治療的研究中,可以看到,對於驅動基因的篩選是關鍵。BR.19研究[2]納入了IB期-IIIA期的肺癌患者,其中>50%的患者為IB期,對比了吉非替尼和安慰劑輔助治療的療效,主要研究終點為OS,研究結果顯示,HR =1.24,P=0.18,為陰性結果。此外,2015年的RADIANT研究[3]也同樣以失敗告終。2018年的一項單臂研究SELECT研究納入了IA期-IIIA期的EGFR陽性患者,接受厄洛替尼術後輔助治療,研究結果顯示,2年的DFS率為88%。
經過了諸多的探索,最終篩選出了可透過術後輔助靶向治療的獲益人群,具有EGFR突變的微小殘留病灶(MRD)陽性患者往往具有較高的復發風險,同時也可以透過EGFR-TKI術後輔助治療獲益。
EGFR-TKI輔助治療交出亮眼成績單
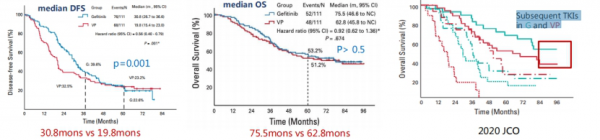
EGFR-TKI在晚期肺癌治療中已經展現出了卓越的治療效果。全球範圍內針對EGFR-TKI術後輔助治療,也進行了漫長的探索。2017年的美國臨床腫瘤學會(ASCO)中,ADJUVANT(CTONG1104)研究[4]證實了術後靶向藥物輔助治療的可行性。隨機、III期臨床試驗ADJUVANT研究探索了第一代EGFR-TKI吉非替尼在可切除的EGFR突變陽性 II-IIIA(N1-N2)期NSCLC患者術後輔助治療中的療效。研究納入222例完全切除的II-IIIA期(N1-N2)EGFR敏感突變的NSCLC患者,入組患者以1:1的比例隨機接受吉非替尼或長春瑞濱聯合順鉑治療。主要研究終點為意向性(ITT)人群的DFS。研究結果顯示,吉非替尼組的疾病復發風險降低44%(HR 0.60,95% CI 0.42-0.87;p=0.0054),吉非替尼術後輔助治療的中位DFS顯著延長達10.7個月(30.8個月 vs 19.7個月),吉非替尼組和化療組的OS無顯著差異。此外,無論是吉非替尼組或是化療組,序貫EGFR-TKI治療均可延長OS。
而IMPACT研究[5]也同樣比較了吉非替尼輔助治療與順鉑聯合長春瑞濱輔助治療的療效,但與ADJUVANT研究相同的是,DFS獲益也未能轉化為OS獲益。
ADUARA研究推動肺癌輔助靶向新格局
近年來,NSCLC輔助治療又有了突破性的進展,隨著第三代EGFR-TKI奧希替尼的ADAURA研究資料公佈[6],奧希替尼輔助治療的療效收到了臨床上的廣泛認可。
研究入組了682例完全切除術後的IB-IIIB期(T3N2,AJCC8)EGFR突變陽性NSCLC患者(無論是否接受輔助化療),分別接受奧希替尼(339例)和安慰劑(343例)治療,主要終點為II/IIIB期(T3N2,AJCC8)患者的無病生存期(DFS)。次要終點為IB-IIIB期(T3N2,AJCC8)患者的DFS、OS和安全性。
結果顯示,在IB期-IIIB期(T3N2,AJCC8)NSCLC患者中,奧希替尼組對比安慰劑組的DFS顯著延長(未達到vs.27.5個月;HR,0.21;P<0.001);在II-IIIB期(T3N2,AJCC8)NSCLC患者中,奧希替尼組與對照組相比也展現出了DFS的優勢(DFS,未達到 vs. 19.6個月;HR,0.17;P<0.001)。此外,奧希替尼組的1年和2年DFS率都顯著優於安慰劑組(97%vs. 61%,90% vs. 44%),3年DFS率差異則超過50%(80% vs.28%)。
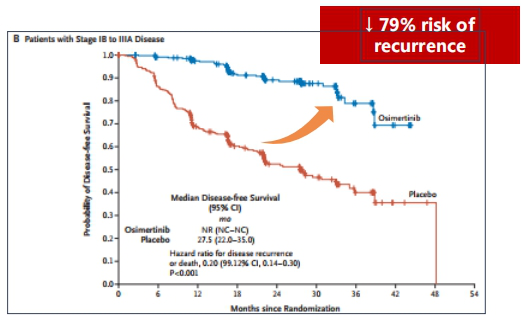
圖3.IB-IIIB期(T3N2,AJCC8)NSCLC患者的DFS
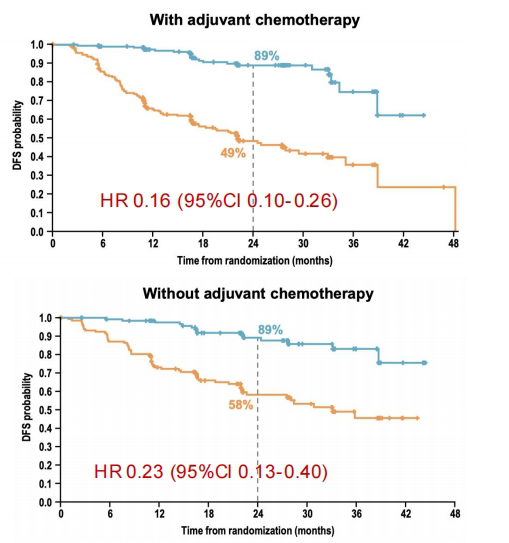
值得關注的是,ADAURA研究顯示,在無論是否接受輔助化療的患者,均可以透過奧希替尼輔助治療獲益。
ADJUVANT研究以及IMPACT研究,均顯示術後靶向輔助治療可以延長患者的DFS,但如何將DFS獲益轉化為OS獲益成為廣大腫瘤內科醫生探索的方向。研究結果顯示,接受輔助化療的結腸癌和肺癌患者OS和DFS之間的呈現出高度的相關性,ADAURA研究最終的OS結果也受到了廣泛的關注和期待。
參考文獻:
[1]Pignon JP, et al. J Clin Oncol, 2008, 26(21):3552-3559.
[2]Goss GD, O'Callaghan c, Lorimer I, etal. Gefitinib versus placebo in completely resected non-small-cell lung cancer:results of the NCIC CTG BR19 study. J Clin Oncol, 2013, 31 ( 27 ):3320-3326.
[3]Kelly K, Altorki NK, Eberhardt WE, etal. Adjuvant Erlotinib versus placebo in patients with stage lB-IIIА nоn-ѕmаll-сеll lung саnсеr ( RАDІАNТ ): а rаndоmіzеd,dоublе-blіnd, рhаѕе III trіаl. J Сlіn Оnсоl,2015, 33 ( 34 ): 4007-4014.
[4]Zhong WZ, Wang Q, Mao WM, et al. Gefitinib versus vinorelbine plus cisplatin as adjuvant treatment for stage II-IIIA (N1-N2) EGFR-mutant NSCLC (ADJUVANT/CTONG1104): a randomised, open-label, phase 3 study. Lancet Oncol. 2018 Jan;19(1):139-148.
[5]Tada, et al. ASCO 2021.
[6]Yi-Long Wu, et al,. 2020 world conference on lung cancer Singapore, OA06
*此文僅用於向醫學人士提供科學資訊,不代表本平臺觀點