源自神經上皮的腫瘤統稱為腦膠質瘤,佔顱腦腫瘤的40%~50%,是最常見的原發性顱內腫瘤。年發病率為3~8人/10萬人口。
今天咱們來了解一下膠質瘤的免疫治療與精準靶向治療的最新進展。
CDK4/6M製劑聯合ERK1/2抑制劑在復發膠質母細胞瘤中的0期觸發試驗
過去50年,僅22項研究在膠質母細胞瘤(GBM)中探索了藥效動力學和/或藥代動力學,0期研究在GBM中明顯未得到充分利用。
雖然CDK4/6抑制劑在Rb基因完好的腫瘤細胞中可破壞細胞週期中的G1期,但已有研究表明CDK4/6抑制劑單藥治療復發、Rb基因完好的GBM的療效並不理想。因此,CDK4/6抑制劑單藥不適用於復發GBM。
研究發現,CDK4/6抑制劑能夠上調復發GBM中的ERK1/2。
研究招募了24名計劃再手術的復發、經過STUPP方案治療的GBM患者,患者的增強腫瘤病灶>1cm3,活檢組織滿足3個標準:1)Rb基因存在表達且無RB基因突變;2)CDKN2A/B/C缺失或CDK4/6擴增;3)PERK表達。
0期試驗中,患者在第1至6天接受150mg的Abemaciclib(CDK4/6抑制劑)+200mg的LY3214996(ERK1/2抑制劑)治療,在第6天進行手術,第一組患者在給藥後7-9小時手術,第二組患者在給藥後3-5小時手術。
安全性方面,70.8%的患者出現不良事件(AE),33.3%的患者出現≥3級不良事件,20.8%的患者出現嚴重不良事件,沒有患者因為不良事件導致劑量中斷或減量,有1名患者因為不良事件退出研究。
II期試驗招募了16名患者,患者接受150mg的Abemaciclib+200mg的LY3214996治療,直到疾病進展。如果16例受試者中有2例的PFS>6個月,則研究人數擴大到25,研究的中位無進展生存期(PFS)為2.4個月。
研究初步得出結論,雖然LY3214996效果有限,但Abemaciclib(CDK4/6抑制劑)與LY3214996(ERK1/2抑制劑)在非增強性GBM中達到了藥理要求的濃度。
基於3名患者治療前的活檢,1名患者的LY3214996的暴露量與ERK1 /2通路抑制有關。
截止目前資料,在PK觸發的II階段患者中,兩藥聯合的中位PFS與瑞博西尼藥相媲美。
CTLA-4單抗聯合PD-1單抗在復發膠質母細胞瘤中顱內注射的I期研究
CheckMate-143 III期研究顯示Nivolumab單藥並未改善復發GBM的總生存,ORR為7.8%;12個月總生存率為41%。
研究的主要終點為安全性/可行性。所有患者都接受了計劃的術前10mg IV NIVO,所有患者都接受了計劃的神經外科手術和研究藥物的圍手術期給藥。
研究未有4-5級AE以及可疑的非預期嚴重不良反應(SUSARs)。未有患者由於irAE需要皮質類固醇(或其他免疫抑制劑)治療。
研究的初步結果表明,顱內注射IPI和NIVO是可行的,且安全性可接受,免疫相關的非預期嚴重不良事件發生率低,且大部分不良事件都是低級別,NIVO在CSV內清除出乎意料地快。
OS的潛在有益影響似乎僅限於可切除的患者,懷疑CNS腫瘤負荷決定治療結果(類似黑色素瘤腦轉移),沒有強有力的跡象表明圍術期注射IPI/NIVO後,重複腔內給藥NIVO會帶來額外好處。
預測/預後組織生物標誌物(包括B7-H3)有潛力指導合適患者篩選,CSV中存在淋巴細胞腫瘤抗原特異性。
正在進一步研究顱內IPI/NIVO給藥設計,以作為新免疫組合治療方案的基礎。
Sorcin的上調將透過啟用PI3K/AKT/mTOR通路促進膠質母細胞瘤進展
Sorcin(SRI)是一種可溶性鈣(Ca2+)結合蛋白,是penta-EF-hand(PEF)蛋白質家族的重要成員,並參與了腫瘤發生。
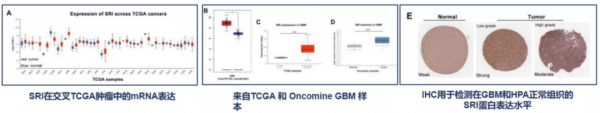
在Oncomine和TCGA資料庫中檢查SRI在GBM中的表達,並透過免疫組織化學染色、western blot和RT-PCR在臨床組織和細胞系中進一步測量。在體外模型中研究了SRI在GBM中的生物學功能,並進一步研究了潛在分子機制。
研究得出結論:
基於各種資料庫,SRI在膠質母細胞瘤(GBM)中表達增加。
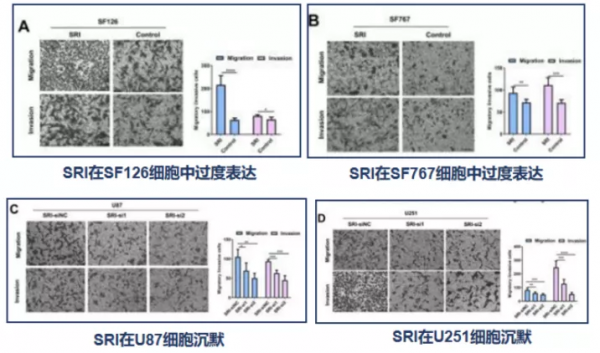
SRI對體外GBM產生影響。
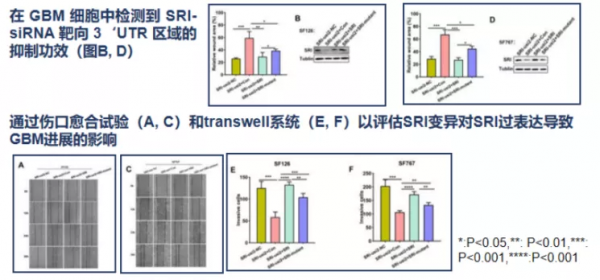
體外模型發現SRI過表達促進GBM遷移和侵襲。
GBM細胞中的EM頂象和P13K/AKT/mT0R通路透過加強SRI表達而增強。
總的來說,上述發現表明SRI在GBM中表達上調,並透過觸發PI3K/AKT/mTOR通路促進GBM進展。
結論
綜上,在PK觸發的I階段患者中,CDK4/6抑制劑聯合ERK1/2抑制劑聯合的中位PFS與瑞博西尼(CDK4/6抑制劑)單藥相媲美。
顱內注射IPI和NIVO是可行的,且安全性可接受,OS的潛在有益影響似乎僅限於可切除的患者。
SRI在GBM中表達上調,並透過觸發PI3K/AKT/mTOR通路促進GBM進展。