NEJM:恩格列淨治療射血分數保留的心衰
在合併2型糖尿病(T2DM)且心臟射血分數降低的心力衰竭患者中,鈉-葡萄糖協同轉運蛋白2(SGLT2)抑制劑可顯著降低心力衰竭發生和發展的風險。然而,目前對於射血分數保留的心衰患者的可選治療方案有限,且缺乏關於SGLT2抑制劑對於此類患者治療作用的大型試驗。
本月The New England Journal of Medicine 釋出了一項隨機、雙盲、安慰劑對照試驗(EMPEROR-Preserved),旨在探討恩格列淨對有或無T2DM的射血分數保留心衰患者的療效。
該研究納入了5988例II-IV級心衰且心臟射血分數>40%的患者,在常規治療的基礎上隨機接受恩格列淨(每日一次,每次10 mg)或安慰劑治療。主要結局為心血管原因死亡或心力衰竭住院構成的複合結局。
經過平均26個月的隨訪,恩格列淨組(n=2997)和安慰劑組(n=2991)中分別發生了415例(13.8%)和511例(17.1%)主要結局事件(HR=0.79,P<0.001),這一效應主要與恩格列淨組因心衰住院風險較低有關(圖1)。在有或無糖尿病的患者中,恩格列淨的治療效果一致。恩格列淨組因心衰住院的總人數少於安慰劑組(恩格列淨組407例;安慰劑組541例,HR=0.73,P<0.001)(圖2)。在藥物不良反應方面,恩格列淨組發生單純性生殖道和尿路感染以及低血壓的風險較高。
圖1. 恩格列淨組和安慰劑組主要結局的累積發生率
本研究表明,在射血分數保留的心衰患者中,不論是否患有糖尿病,恩格列淨均可降低心血管死亡或因心力衰竭住院的複合風險。恩格列淨對於此類患者的獲益與對射血分數保留的心力衰竭患者開展的平行試驗(EMPEROR-Reduced)的結局報道一致,提示SGLT2抑制劑對於心力衰竭的治療效應並未因心衰的表型不同而顯著改變,具有良好的臨床應用前景。
全文資源:
https://www.nejm.org/doi/full/10.1056/NEJMoa2107038
BMJ:增加亞麻酸攝入與心血管疾病和死亡風險降低有關
α-亞麻酸(ALA)是一種主要存在於堅果和種子等食物中的多不飽和脂肪酸,是人體腦細胞和組織細胞的重要組成成分。ALA可透過抗炎作用起到預防心血管疾病(CVD)和癌症的效應,但關於ALA攝入與死亡風險的報道較少。
本月BMJ 釋出了一項系統綜述和薈萃分析,旨在全面探討ALA對於心血管死亡、全因死亡和癌症死亡風險的影響。
研究納入了41項關於ALA攝入與全因死亡、心血管死亡和癌症死亡的佇列研究,共1 197 564名研究物件。隨訪時間為2-32年,期間共發生198 113例死亡事件,包括62 773例心血管死亡和65 954例癌症死亡。
與攝入ALA水平較低組(0.73g/天)相比,攝入ALA水平較高組(平均1.59g/天)全因死亡(RR=0.90)、CVD死亡(RR=0.92)和冠心病死亡(RR=0.89)風險降低,但癌症死亡風險(RR=1.06)輕度增加。劑量反應分析發現,每日增加1 g的ALA攝入與全因死亡風險降低5%和CVD死亡風險降低5%有關。血中ALA水平每增加1個標準差,冠心病(CHD)死亡風險降低8%(圖1)。
圖1. ALA每日攝入量與全因死亡、心血管疾病死亡、冠心病死亡和癌症死亡率的劑量反應關係
該研究表明,增加ALA攝入量與全因死亡風險降低、CVD風險降低和癌症死亡風險輕度升高有關,而血中ALA水平較高與全因死亡和CHD死亡風險降低有關。為確定每日最佳ALA攝入量,應進一步探討ALA與其他原因死亡之間的關聯,並納入關於亞洲人群的結局評估。
全文資源:
https://www.bmj.com/content/375/bmj.n2213
Lancet 內分泌子刊:達格列淨可降低慢性腎病患者的尿蛋白量
慢性腎病(CKD)是一種進行性腎功能減退,最終可進展為腎衰並需要透析和腎移植治療。蛋白尿是CKD患者發生腎衰和心血管事件的已知危險因素之一,臨床研究顯示服用達格列淨(一種SGLT2抑制劑)可改善合併2型糖尿病(T2DM)的CKD患者的蛋白尿情況。
本月The Lancet Diabetes & Endocrinology 釋出了一項多中心、雙盲、安慰劑對照的隨機試驗(DAPA-CKD試驗)[1],旨在探討達格列淨對於對於合併或未合併T2DM的CKD患者的治療效果有無差異。
研究納入了eGFR 25-75 mL/min·1.73 m2、尿蛋白肌酐比值(UACR)200-5000 mg/g的慢性腎病患者,隨機接受10 mg/日的達格列淨治療或安慰劑治療,預設結局為蛋白尿的改變,附加結局為UACR分期的進展。
最終達格列淨組和安慰劑組各納入了2152名患者,中位UACR為949 mg/g。與安慰劑組相比,達格列淨組的平均UACR降低了29.3%。在合併和未合併T2DM的患者中,達格列淨組的平均UACR分別較安慰劑組降低35.1%和14.8%(圖1)。在3860名基線UACR≥300 mg/g的患者中,服用達格列淨增加了UACR分期降低(由大量蛋白尿轉為微量蛋白尿或無蛋白尿)的比例(HR=1.81);在3820名基線UCR 300 mg/g以下的患者中,達格列淨降低了UACR分期進展的風險(HR=0.41)。達格列淨治療第14天的UACR降低幅度與隨訪期間eGFR降低減慢有關。

圖1. 全部(A)、合併T2DM(B)和未合併T2DM(C)患者中,達格列淨組和安慰劑組的UACR隨時間的變化
該研究表明,達格列淨可顯著降低CKD患者的蛋白尿水平,並且在合併T2DM的患者中效果更明顯。同期發表的一項研究也顯示,達格列淨延緩CKD患者腎功能衰退的效果在合併T2DM的患者中更為明顯[2]。因此,在使用達格列淨對有或無T2DM的CKD患者進行治療時,可能需要應用不同的給藥方案。
全文資源:
1.https://www.thelancet.com/journals/landia/article/PIIS2213-8587(21)00243-6/fulltext
2.https://www.thelancet.com/journals/landia/article/PIIS2213-8587(21)00242-4/fulltext
JAMA 子刊:孕期糖尿病與後代精神疾病風險增加有關
糖尿病是女性圍生期常見代謝性疾病之一,並且近年來患病率顯著增加。流行病學調查顯示母親妊娠期間患有糖尿病可能增加後代發生注意缺陷與多動障礙風險,但對於妊娠期間糖尿病和後代精神疾病風險的研究證據較少。
本月JAMA Netw Open 釋出了一項基於人群的佇列研究,旨在探討母親妊娠期間或孕前患有糖尿病與其後代四十歲前患有精神疾病的關聯。
研究基於幾項丹麥國家佇列,納入1978-2016年出生,且母親在妊娠期間或孕前患有糖尿病的個體。研究的主要結局包括10種精神疾病:任何精神疾病、藥物濫用、精神分裂、心境障礙、焦慮症、進食障礙、人格障礙、智力障礙、發育障礙和行為障礙。
最終納入了2 413 335名研究物件,平均年齡19歲。經過39年的隨訪,151-208名(6.4%)物件被診斷患有精神疾病。與母親妊娠期間無糖尿病的個體相比,母親妊娠期間患有糖尿病的物件發生任何精神疾病(HR=1.15)、精神分裂(HR=1.55)、焦慮(HR=1.22)、智力障礙(HR=1.29)、發育障礙(HR=1.16)、行為障礙(HR=1.17)的風險不同程度地增高(圖1)。但母親糖尿病與後代藥物濫用、心境障礙、進食障礙和人格障礙無關。亞組分析顯示,母親孕前患有糖尿病、妊娠期間患有糖尿病、患T1DM或T2DM時,個體發生精神疾病的風險均增高。
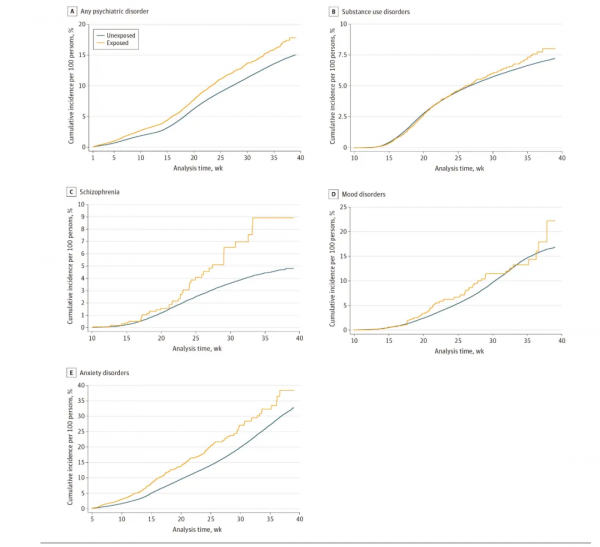
圍生期有或無糖尿病與後代精神疾病(A)、物質濫用(B)、精神分裂(C)、心境障礙(D)焦慮症(E)的關聯
該研究表明,母親圍生期糖尿病與後代患有多種精神疾病的風險增加有關。未來有必要探討其他人群中母親糖尿病與後代精神健康的關聯,並加強對育齡期女性的糖尿病早期篩查和預防。
全文資源:
https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2784997
NEJM:基因測序揭示GNAS突變相關肥胖的臨床表現差異
GNAS基因編碼刺激性G-蛋白α亞單位(Gαs),參與G蛋白偶聯受體的訊號轉導途徑。GNAS突變可導致Albright遺傳性骨營養不良綜合徵,以發育遲緩、身材矮小和骨骼發育異常為主要特徵。此外,母體等位基因的突變也可能導致肥胖和激素抵抗(假性甲狀旁腺功能減退)。
本月The New England Journal of Medicine 釋出了一項佇列研究,旨在探討GNAS突變對於G蛋白偶聯受體訊號通路的不同影響,是否與患者假性甲狀旁腺功能減退臨床表現的異質性有關。
該研究對2548例嚴重肥胖的患者進行了外顯子測序和定向重新測序,共發現22名GNAS突變的攜帶者。研究者分析了GNAS突變相關肥胖是否與黑皮質素受體4(MC4R)訊號通路異常有關,以及分子檢測結果能否解釋患者臨床表現的不同。
結果表明,幾乎所有GNAS突變的患者都存在MC4R訊號通路的異常。11名年齡12至18歲的患者中,共有6名患者的GNAS突變干擾了生長激素釋放激素受體通路,出現生長髮育不良;但在該訊號通路未受到影響的突變攜帶者中,生長髮育情況正常(身高平均標準偏差分別為-0.90和0.75,P =0.02)。
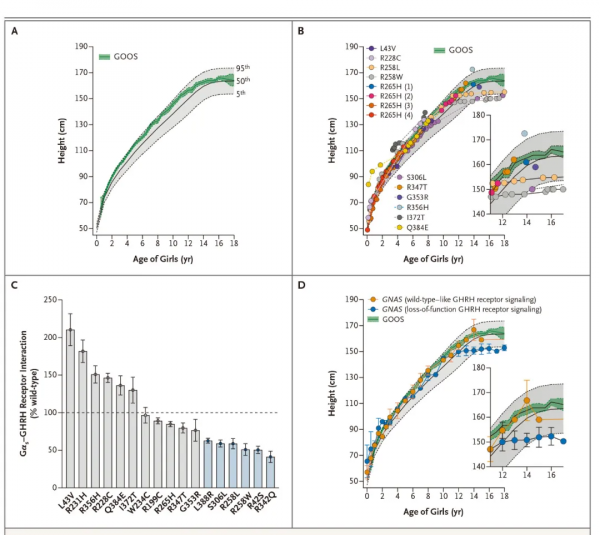
在研究前或研究期間達到最終身高的10名患者中,僅有1名身材矮小(圖1)。與340名未發生GNAS突變的嚴重肥胖兒童(3.9±2.6 mIU/L)相比,損害甲狀腺激素受體訊號的GNAS突變與發育遲緩有關,且患者促甲狀腺激素水平較高(8.4±4.7 mIU/L)。
*注:圖A為入組的2529名肥胖女性的平均身高;圖B為GNAS突變攜帶者的平均身高;圖C為功能性研究報道的GHRH受體與Gαs相互作用情況;圖D為不同效應的GNAS突變攜帶者的平均身高。
該研究表明,GNAS突變患者可僅表現為肥胖,並且存在MC4R通路的異常。GNAS突變對於GPCR訊號通路的不同影響,可導致不同的臨床表現。因此對嚴重肥胖的患者進行GNAS突變和相關激素抵抗的篩查,或許有助於假性甲狀旁腺功能減退的早期診斷。
原文連結:
https://www.nejm.org/doi/full/10.1056/NEJMoa2103329
文/付金蓉 中國醫科大學附屬第一醫院;關海霞 廣東省人民醫院
責編/Jane