10月12日,vTv Therapeutics宣佈TTP399治療I型糖尿病的機制研究獲得積極結果,證明接受TTP399治療的1型糖尿病患者在退出胰島素治療期間相比安慰劑組沒有發生酮酸水平增高,意味著TTP399不增加酮酸中毒的風險。
該機制研究入組23例正在使用胰島素泵的1型糖尿病患者,隨機分組接受每日1次TP399 (n=12)或安慰劑 (n=11) ,為期大約7天。在完成最後一天給藥後讓患者停止使用胰島素泵,以進行胰島素急性撤除測試,檢測最多10小時內或滿足特定安全性事件標準前的β-羥基丁酸(BOHB)和其他代謝標誌物的水平。
與之前的研究一致,TTP399能夠改善空腹血糖控制,並且TTP399治療組在胰島素撤除測試前1周發生沒有低血糖事件,安慰劑對照組有4例低血糖事件。
FDA此前拒絕批准SGLT-2抑制劑作為T1D患者的輔助療法,主要是擔心發生糖尿病酮酸中度(DKA)的風險。DKA一旦發生,需要住院治療,如果不及時處理,會有死亡風險。為了回應FDA對藥物安全性方面的關切, vTv Therapeutics應FDA要求開展TTP399此項機制研究,以證明TTP399不會導致酮酸產生而繼發DKA。
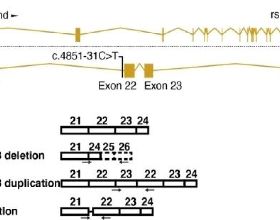
TTP399是一種選擇性葡萄糖激酶激動劑,曾憑藉II期SimpliciT-1試驗(NCT03335371)結果獲得FDA授予的治療1型糖尿病的突破性療法,相比安慰劑將HbA1c顯著降低0.21%,並將嚴重和症狀性低血糖發生率降低40%。vTv Therapeutics計劃2022年初啟動TTP399的III期研究。