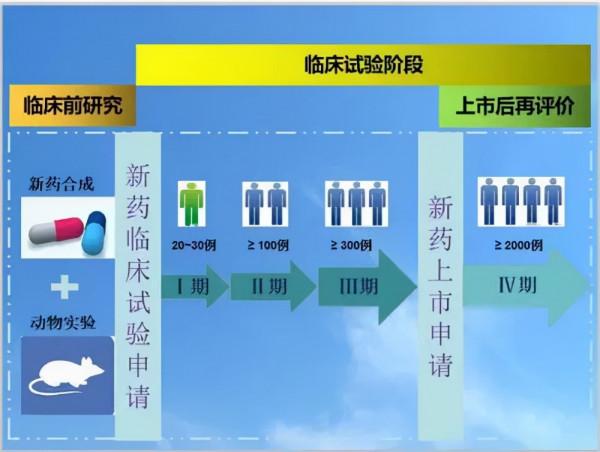
Antios Therapeutics公司與Assembly Biosciences公司旗下正有兩款在研乙肝新藥,即ATI-2173和Vebicorvir,兩家藥企將正在進行的Antios IIa期 ANTT201研究中開闢一個單一佇列,來評估ATI-2173+Vebicorvir+富馬酸替諾福韋二吡呋酯(TDF)三聯療法!
乙肝研究藥企合作,ATI-2173+VBR+TDF,2022年上半年開始
這是一項剛剛宣佈的全球慢乙肝新藥之間的聯合給藥試驗,ATI-2173,是Antios公司正在開發的專有活性位點聚合酶抑制劑核苷酸(ASPIN),vebicorvir (VBR)是Assembly Bio公司正在臨床開發中的在研先導核心抑制劑候選藥物,富馬酸替諾福韋二吡呋酯(TDF)是一款全球已經獲批的核苷酸逆轉錄酶抑制劑。這項 IIa期其中一個單一佇列,會評估上述研究藥物之間的聯合療法。
一、兩家藥企科學家點評
來自Antios公司的執行長Gregory Mayes點評:Antios公司專注於為慢性HBV感染者開發一種可能實現功能性治癒療法。迄今為止,ATI-2173已證明具有普遍良好的安全性和耐受性,在其臨床開發中,ATI-2173利用獨特的 ASPIN機制為HBV聯合療法提供支援。最終,ATI-2173有可能成為每日1次與其他藥物(vebicorvir)聯合治療慢性HBV感染者的基石治療方案。
來自Assembly Bio公司的執行長兼總裁,醫學博士John McHutchison點評:這次我們與Antios公司的乙肝新藥臨床開發合作,強調了我們致力於評估管線中的HBV核心抑制劑和核苷(酸)類似物(NAs)為骨架,並結合其他機制在研新藥來治療HBV的潛力。這是一種慢性感染的主要原因,可導致更高的 LC 和HCC發生風險。
我們與Antios公司共同致力於為HBV患者,開發出一種有限療程來實現功能性治癒的新療法,我們的科研團隊共同為這項研究工作,併為HBV患者帶來希望。
二、新增試驗設計基本方案
這是將是一項多中心、雙盲、安慰劑對照佇列來評估這種全口服三聯療法的安全性、藥代動力學(PK)和抗病毒活性。預計這個新增三聯療法將在2022年上半年開始,並將在為期12周的治療研究中,納入10名初治或停止治療的乙肝e抗原(HBeAg)陰性或陽性患者。
三、vebicorvir(以往稱ABI-H0731)和ATI-2173作用機理及以往表現
Assembly Bio公司的乙肝在研新藥組合,現有三種小分子候選藥物,它們都是針對乙肝病毒複製週期多個步驟的HBV核心抑制劑。在 II期臨床試驗中,該公司第一代核心抑制劑vebicorvir(VBR)+核苷(酸)類似物顯示出良好安全性,相較於使用核苷類似物的單藥治療方案,這種組合療法可導致 HBVDNA和 HBV pgRNA的更明顯病毒抑制效果。
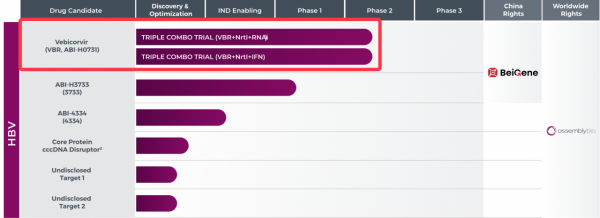
來自:Assembly Bio公司管線,紅色備註是VBR原來已有兩個II期組合研究
目前,Assembly Bio公司的這款HBV核心抑制劑正在進行多項 II期聯合用藥研究。我們能夠從該公司管線更新看到,VBR已經處在 II期的組合研究有兩個,即VBR+核苷酸逆轉錄酶抑制劑(Nrtl)+RNAi,VBR+Nrtl+IFN,隨著上述兩家藥企推出臨床合作計劃,VBR還會在新增一項組合研究,即VBR+ATI-2173+TDF。
ATI-2173,是一款被設計用於治療HBV按照每日1次的口服藥物,它的作用機理是尋求和其他不同作用機制藥物進行互補組合研究來尋求實現功能性治癒。
小番健康結語:目前,這兩款在研乙肝新藥都處在 II期臨床試驗中。這是一項剛剛宣佈的臨床開發合作專案,從Antios公司的角度,將正在進行的 IIa期ANTT201臨床試驗中,開闢出一個單一佇列來評估三聯療法:ATI-2173+VBR+TDF。當然,這項新藥組合研究會在2022年上半年才啟動。