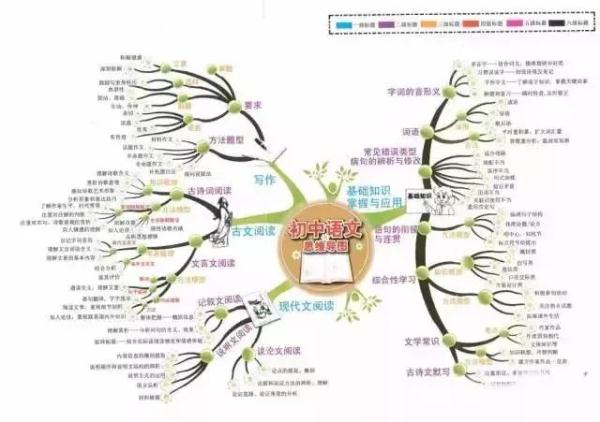
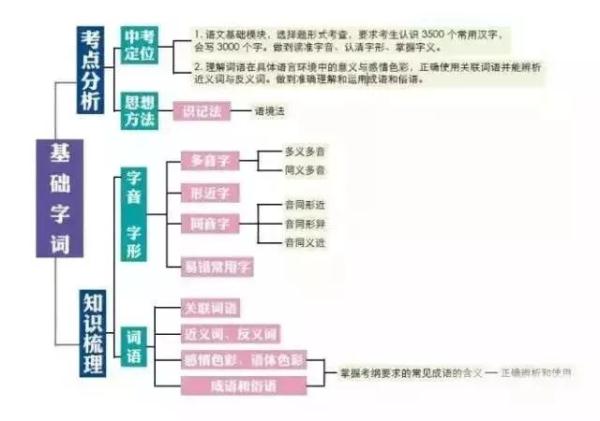
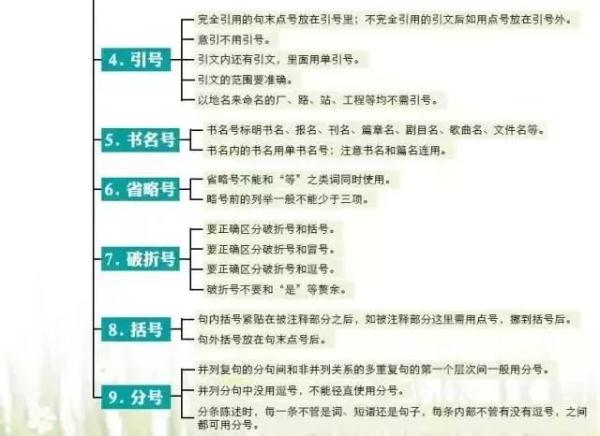
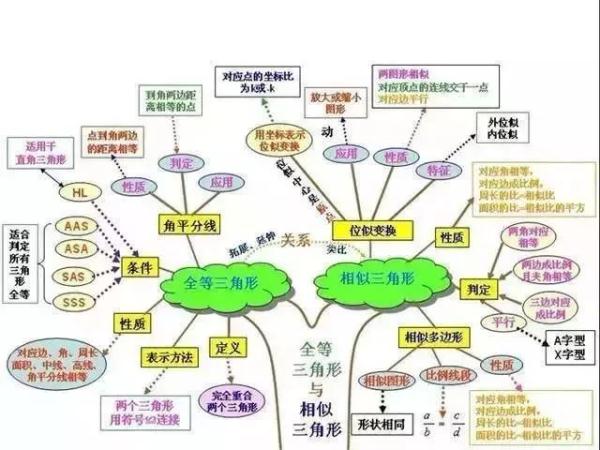
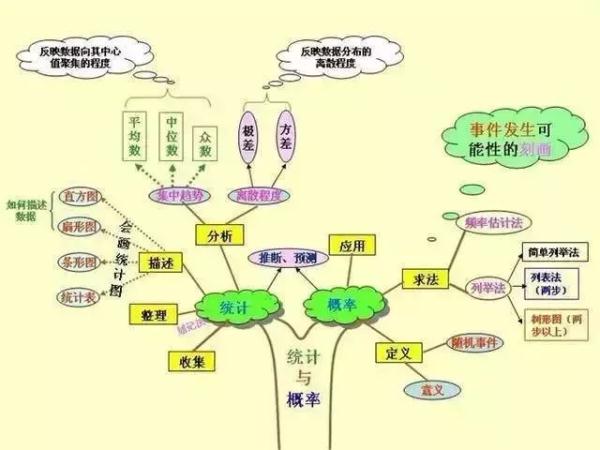
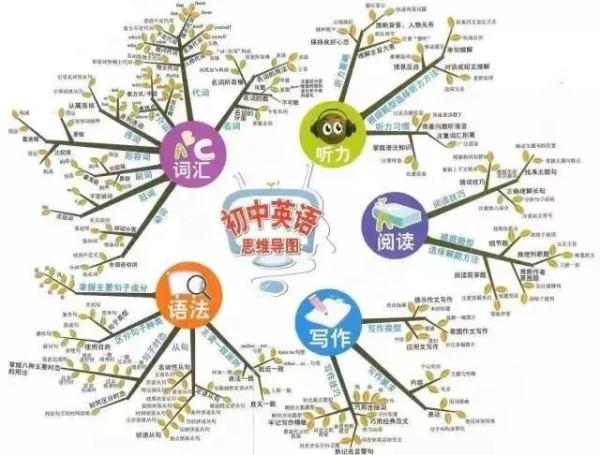
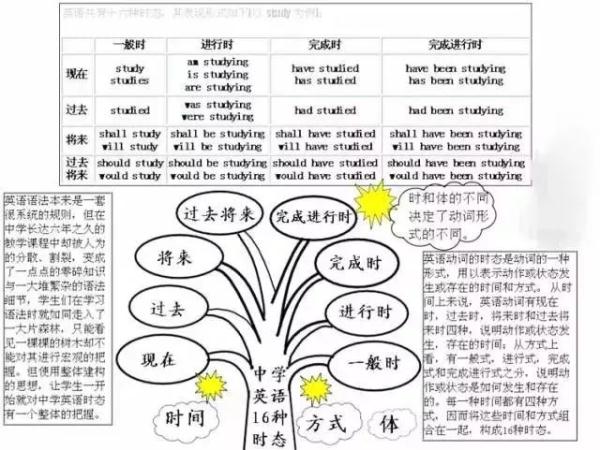
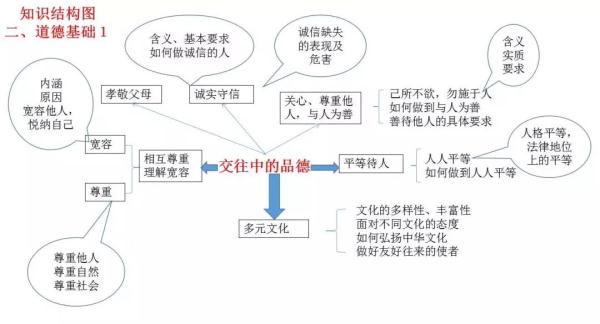
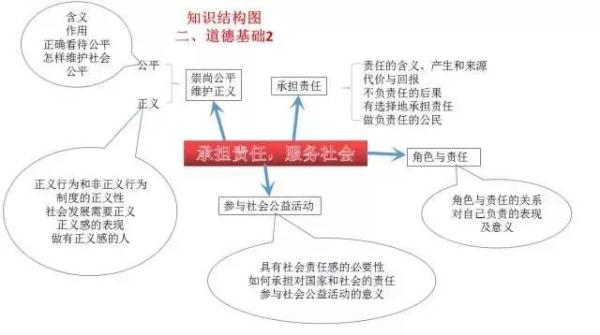
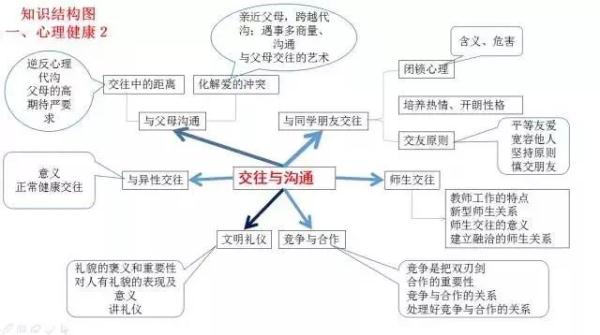
初中與小學相比,科目更多了,需要學習的內容也更多了,學習壓力更大。各科都有知識量大、系統性強、綜合性強以及能力要求高等特點,知識點是零亂的,不利於記憶和掌握。
然而,學霸們能學習好,自然有自己的方法。一位女學霸就用“紅線”把知識“串”起來,這樣,各科知識結構就一目瞭然了。
今天,把這位女學霸的知識總結分享給大家,方便同學們整體把握知識之間的聯絡。如果都掌握了,你的學習成績一定會更上一層樓!!
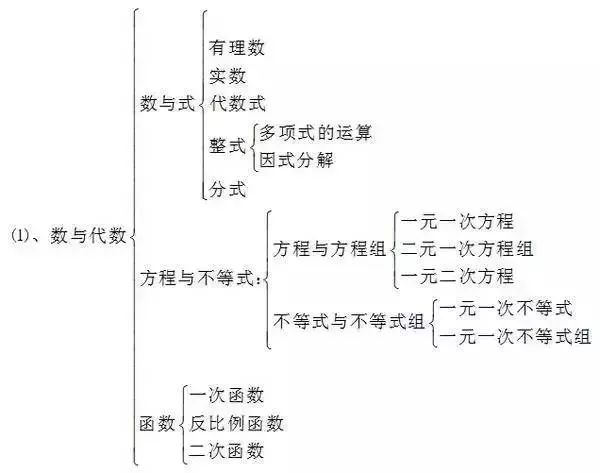
1、代數式
一、地球和地圖
二、陸地和海洋
三、天氣與氣候
四、居民與聚落
五、發展與合作
六、亞洲
七、鄰近的地區和國家
八、東半球的其他的地區和國家
九、西半球的國家
十、極地地區
十一、從世界看中國
十二、中國自然環境
十三、中國的自然資源
十四、中國的經濟發展
十五、中國的地理差異
十六、北方地區
十七、南方地區
十八、西北地區
十九、青藏地區
二十、中國在世界中
物理
化學
第一單元 走進化學世界
第二單元 我們周圍的空氣
第三單元 自然界的水
第四單元 物質構成的奧秘
第五單元 化學方程式
第六單元 碳和碳的氧化物
第七單元 燃料及其利用
第八單元 金屬和金屬材料
九、溶液
一、化學用語
1、電離方程式
2、物質的俗稱和主要成分:
生石灰CaO;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食鹽的主要成分NaCl ;純鹼、口鹼Na2CO3;燒鹼、火鹼、苛性鈉NaOH;膽礬、藍礬CuSO4.5H2O;碳酸鈉晶體Na2CO3.10H2O;氨水NH3.H2O;
二、金屬活動性
1、金屬活動性順序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au
2、金屬活動性順序的意義:在金屬活動性順序中,金屬位置越靠前,金屬在水溶液(酸溶液或鹽溶液)中就越容易失電子而變成離子,它的活動性就越強。
3、金屬活動性順序的應用:
(1)排在氫前的金屬能置換出酸裡的氫(元素)。
(2)排在前面的金屬才能把排在後面的金屬從它們的鹽溶液中置換出來(K、Ca、Na除外)。
三、酸、鹼、鹽的溶解性
1、常見鹽與鹼的溶解性:
鉀(鹽)、鈉(鹽)、銨鹽全都溶,硝酸鹽遇水影無蹤。
硫酸鹽不溶硫酸鋇,氯化物不溶氯化銀。
碳酸鹽只溶鉀(鹽)、鈉(鹽)、銨(鹽)。
鹼類物質溶解性:只有(氫氧化)鉀、(氫氧化)鈉、(氫氧化)鈣、(氫氧化)鋇溶。
2、八個常見的沉澱物:氯化銀、硫酸鋇碳酸銀、碳酸鋇、碳酸鈣、氫氧化鎂、氫氧化銅、氫氧化鐵
3、四微溶物:
Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(實驗室制二氧化碳時不用稀硫酸的原因)
Ag2SO4(鑑別SO42-和Cl-時,不用硝酸銀的原因)、MgCO3(碳酸根離子不能用於在溶液中除去鎂離子的原因)
4、三個不存在的物質:氫氧化銀、碳酸鋁、碳酸鐵
四、複分解反應發生的條件反應
有氣體、水或沉澱生成(即有不在溶液中存在或在水溶液中不易電離的物質)
(1)不溶性鹼只能與酸性發生中和反應
(2)不溶性鹽,只有碳酸鹽能與酸反應(3)KNO3、NaNO3、AgNO3、BaSO4不能做複分解反應的反應物
五、溶液的酸鹼性與酸鹼度的測定
1、指示劑---溶液的酸鹼性紫色的石蕊試液遇酸性溶液變紅;遇鹼性溶液變藍
無色的酚酞試液只遇鹼溶液變紅 注:不溶性鹼與指示劑無作用;鹼性溶液不一定是鹼的溶液(特例:碳酸鈉的水溶液顯鹼性)
2、pH值---溶液的酸鹼度:pH<7溶液為酸性(越小酸性越強);ph=7溶液為中性;ph>7溶液為鹼性(越大鹼性越強)
六、離子的檢驗
Cl-(在溶液中)---在被測溶液中加入硝酸銀溶液,如果生成不溶於硝酸的白色沉澱,則原被測液中含氯離子。
SO42-(在溶液中)---在被測溶液中加入氯化鋇(或硝酸鋇、或氫氧化鋇)溶液,如果生成不溶於硝酸(或鹽酸)的白色沉澱,則原被測液中含硫酸根離子。
CO32-
(1)(固體或溶液)---在被測物質中加入稀酸溶液,如果產生能使澄清石灰水變渾濁的氣體,則原被測物質中含碳酸根離子。
(2)(在溶液中)---在被測溶液中加入氯化鋇或硝酸銀溶液,如果產生能溶於硝酸的白色沉澱,且同時生成能使澄清的石灰水變渾濁的氣體,則原被測溶液中含碳酸根離子。
( 注:1、在鑑別Cl-和SO42-時,用氯化鋇溶液,不要用硝酸銀溶液,這是因為硫酸銀為微溶性物質,使鑑別現象不明顯;2、在一未知溶液中加入氯化鋇溶液,若產生不溶於硝酸的白色沉澱,則原被測液中可能含銀離子也可能含硫酸根離子。)
七、物質的顏色
1、固體(多為白色)
黑色---CuO、C粉、MnO、2Fe3O4、
紫黑色---KMnO4
紅色---Cu、Fe2O3
紅褐色---Fe(OH)3
藍色---Cu(OH)2、CuSO4.5H2O
綠色---Cu2(OH)2CO3
2、溶液(多為無色):
淺綠色溶液---(亞鐵鹽溶液)FeCl2溶液、FeSO4;
黃色溶液--- (鐵鹽溶液)FeCl3溶液、Fe2(SO4)3溶液、Fe(NO3)3
溶液藍色溶液---(銅鹽溶液)CuCl2溶液、CuSO4溶液、Cu(NO3)2
溶液藍綠色溶液---CuCl2溶液(較濃)
八、酸、鹼、鹽的特性
1、濃鹽酸---有揮發性、有刺激性氣味、在空氣中能形成酸霧。
2、濃硝酸---有揮發性、有刺激性氣味、在空氣中能形成酸霧,有強氧化性。
3、濃硫酸---無揮發性。粘稠的油狀液體。有很強的吸水性和脫水性,溶水時能放出大量的熱。有強氧化性。
4、氫氧化鈣---白色粉末、微溶於水。
5、氫氧化鈉---白色固體、易潮解,溶水時放大量熱。能與空氣中的二氧化碳反應而變質。
6、硫酸銅---白色粉末、溶於水後得藍色溶液(從該溶液中析出的藍色晶體為五水合硫酸銅CuSO4.5H2O)。
7、碳酸鈉---白色粉末,水溶液為鹼性溶液(從溶液中析出的白色晶體為碳酸鈉晶體Na2CO3.10H2O)
8、氨水(NH3.H2O)---屬於鹼的溶液
九、酸與鹼的通性和鹽的性質
1、酸的通性
(1)酸溶液能使紫色的石蕊試液變紅,不能使無色的酚酞試液變色。
(2)酸能與活潑金屬反應生成鹽和氫氣
(3)酸能與鹼性氧化物反應生成鹽和水
(4)酸能與鹼反應生成鹽和水
(5)(5)酸能與某些鹽反應生成新的鹽和新的酸
2、鹼的通性
(1)鹼溶液能使紫色的石蕊試液變藍,並能使無色的酚酞試液變紅色
(2)鹼能與酸性氧化物反應生成鹽和水
(3)鹼能與酸反應生成鹽和水
(4)某些鹼能與某些鹽反應生成新的鹽和新的鹼
3、鹽的性質
(1)某些鹽能與較活潑的金屬反應生成新的鹽和金屬
(2)某些鹽能與酸反應生成新的鹽和新的酸
(3)某些鹽能與某些鹼反應生成新的鹽和新的鹼
(4)有些不同的鹽之間能反應生成兩種新的鹽
生物
(轉自:廣州品學)
來源: 新父母線上