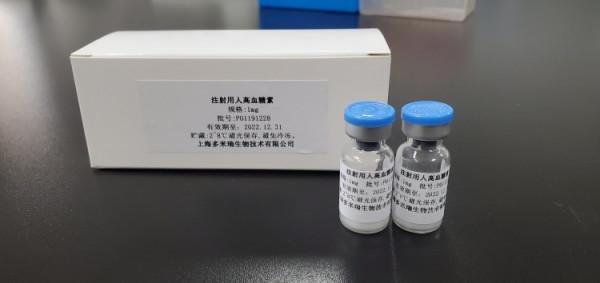
近日,位於浦東張江的上海多米瑞生物技術有限公司,正在著手準備“注射用人高血糖素”臨床樣品的生產,爭取儘快推進該產品的臨床試驗以及後續產業化程序,早日實現該款國產藥上市。

記者瞭解到,國藥醫工總院下屬的上海多米瑞生物技術有限公司已收到國家藥品監督管理局核准簽發的“注射用人高血糖素”藥物臨床試驗批准通知書。該產品不僅是全球首個按生物類似藥開發的人高血糖素產品,而且也是多米瑞公司自行開發並獲批臨床的首個產品,具有里程碑式意義。該產品的獲批,充分說明多米瑞公司已具備獨立開展藥品臨床前研究的能力,正式邁入自主開發產品的新階段。
我國糖尿病患者數量高達1.3億,患者規模和發病率均居世界首位,是糖尿病最嚴重的國家。胰島素是最有效的糖尿病治療藥物,對於I型糖尿病患者來說,胰島素是唯一的治療藥物。低血糖是糖尿病患者治療過程中常見的併發症之一,特別是在胰島素強化治療中極易發生,一旦形成嚴重低血糖,患者會出現意識喪失甚至危及生命。人高血糖能在幾分鐘內將血糖升至正常水平,因此是治療嚴重低血糖最有效的藥物,扮演著“急救藥”“救命藥”的角色,同時在胃腸道檢查和評估胰島β細胞功能等臨床診斷中也有顯著優勢。2016年國家衛計委、工信部、藥監局聯合釋出的《首批鼓勵研發申報兒童藥品清單》就明確將高血糖素作為鼓勵研發品種。
多米瑞公司總經理馮軍研究員表示,儘管進口產品在國內已上市多年,但該藥的國產生物類似藥始終未上市,並且進口產品還存在供應短缺的現象,屬於臨床亟需藥物。同時原研產品採用重組DNA技術生產,作為生物類似藥進行開發具有較高的技術門檻。“我們多年來深耕多肽藥物領域,這款產品也獲得國家‘十三五’重大新藥創制科技重大專項支援。”
據預測,人高血糖素2021年全球銷售額將超6億美元,並且逐年升高,同時其在人工胰腺等新的糖尿病治療方案中也展現了良好的應用前景,在我國也存在巨大的市場潛力和未被滿足的臨床需求。馮軍研究員表示:“醫工總院正在幫助多米瑞公司解決臨床樣品及商業化生產基地的問題,以推進該產品的臨床試驗以及後續產業化程序,早日實現該藥上市。”
欄目主編 許素菲
責任編輯 鄧清元
攝影 路建光