含氯天然產物因其獨特的生物活性受到有機合成化學家的關注,同時含氯甾體藥物作為一類重要的合成甾體在臨床上廣泛應用,因此發展高效的合成策略實現含氯甾體分子的簡潔、精準合成具有重要的研究意義。Clionastatins A和B是義大利科學家Fattorusso等於2004年在海洋穴居海綿Cliona nigricans中分離出的一類多氯代甾體天然產物,具有良好的抗腫瘤細胞毒性(IC50 = 0.8-2.0 μg/mL)。它們是首例從自然界中分離出的多滷代甾體天然產物,且分子中氯原子不以常見的氯醇形式存在。由於分離得到的天然產物量較少(每個天然產物僅分離得到1 mg左右的樣品),其化學結構僅透過核磁譜圖確定;同時分離文獻中未報道天然產物的單晶結構和核磁碳譜譜圖,而僅是透過二維核磁譜圖HSQC和HMBC完成了碳譜化學資料的指定,因此其報道的化學結構和碳譜資料的準確性需要進一步透過化學合成的手段鑑定。
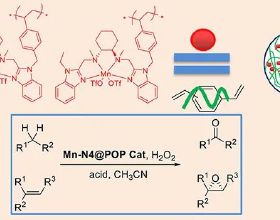
中國科學院上海有機化學研究所天然產物有機合成化學院重點實驗室桂敬漢課題組致力於活性甾體和萜類天然產物的高效合成研究,以往研究發展了基於骨架可控性重組的仿生合成策略,實現了多個複雜甾體天然產物的高效合成(J. Am. Chem. Soc. 2018, 140, 9413/2019, 141, 5021/2020, 142, 5007/2021, 143, 4886;Angew. Chem. Int. Ed. 2021, 60, 11222)。近日,該課題組報道了多氯代甾體天然產物clionastatins A和B的首次全合成與其結構的修正(J. Am. Chem. Soc.2021,DOI:10.1021/jacs.1c07511)。基於天然產物結構的分析,研究指出這類天然產物合成的難點在於:根據Furst-Plattner規則,即環己烯的雙滷代反應傾向於給出雙直立鍵產物,因此clionastatins中處於準平伏鍵C1和C2雙氯原子的立體選擇性引入頗具挑戰;分子中存在非常獨特、高度不飽和的3,5,8,16-四烯-7,15-雙酮結構,易於發生B環的芳構化反應,因此,如何選擇合適的時機引入B環的不飽和結構同時避免其發生芳構化反應較為重要;天然產物報道結構的不確定性增加了合成的難度。
研究從已知烯酮化合物出發,CBS還原和Ireland-Claisen重排反應實現了手性醯基自由基前體的製備,並將產生的C1手性立體化學轉移至C5位;醯基自由基共軛加成反應和分子內Heck反應構築了天然產物核心的四環骨架結構,並將C5手性立體化學轉移至C10位,得到了正確構型的C10季碳手性中心;亞磺酸內酯底物控制的烯烴雙氯代反應引入了挑戰性的C1和C2準平伏鍵雙氯原子,脫氫反應消除C5手性中心,以16-17步反應完成了clionastatins A 和B的首次全合成。合成樣品的NOE譜圖和clionastatin A的單晶結構均顯示,天然產物的C/D環是順式稠合的方式(即C14-H處於β構型),而不是文獻報道的反式稠合的結構(即C14-H處於α構型),糾正了文獻中錯誤報道的天然產物結構。整個合成過程中,科研人員使用了無痕立體化學傳遞(traceless stereochemical relay)的策略,即由CBS還原反應、Ireland-Claisen重排反應和分子內Heck反應實現了C10位季碳手性中心的精準構建。該研究展示了匯聚式合成策略在複雜天然產物合成中的高效性,並體現了天然產物合成目前仍是複雜分子結構鑑定或修正的重要手段。
研究工作得到國家自然科學基金委員會和上海市科學技術委員會的資助。

多氯代甾體天然產物clionastatins A和B的首次全合成
來源:中國科學院上海有機化學研究所