秦天課題組Nat. Chem.:遇水架橋—分子內偶聯合成多取代雙環烷基硼酸酯
本文來自微信公眾號:X-MOLNews
眾所周知,籠狀雙環分子憑藉其特殊的幾何形狀、物理性質以及理論意義等特性,長期以來一直是科學家們的研究熱點。近年來,藥物化學家發現籠狀雙環分子具有調節候選藥物藥代動力學和理化性質的能力(圖1a),並在藥物研發中取得了顯著的成效。其中雙環[1.1.1]戊烷(BCPs)被廣泛認為是苯環的生物電子等排體,而當BCPs上的橋頭位置(C1與C3)被取代時,即可獲得一系列籠狀雙環骨架(圖1b)。目前,構建BCPs的方法主要有以下幾種:1)Wiberg、Michl、Baran等人以高張力[1.1.1]螺槳烷6為原料,經單電子或雙電子轉移途徑獲得對稱與不對稱BCPs(圖1c),該策略主要製備C1和/或C3取代的BCPs;2)構建C2取代BCPs骨架的策略,如Wurtz偶聯、Norrish–Yang環化、[2 + 2]光環加成、環收縮以及擴環反應。然而,這些策略通常會存在底物範圍受限以及產率較低等問題。因此,迫切需要開發一種快速高效的方法來構建多取代(C1、C2與C3)BCPs分子。
近日,美國德克薩斯大學西南醫學中心的秦天教授課題組從硼酸酯取代的環丁酮出發,經分子內偶聯成功地構建了一系列多取代BCPs(圖1d),同時還製備了多種結構複雜的雙環烷基硼酸酯,特別是橋頭烷基硼酸酯還能進行後續的衍生化。如圖1d所示,硼酸酯取代的環丁酮9與活化劑磺醯肼原位生成環丁烷連線的磺醯腙和硼酸酯,後者經鹼介導的分子內偶聯得到高活性的雙環[2.1.1]兩性離子中間體10,隨後經1,2-金屬酸鹽重排、N2釋放便可形成所需的BCP骨架11。相關成果發表在Nature Chemistry 上。
圖1. 橋連烴和 BCP 合成。圖片來源:Nat. Chem.
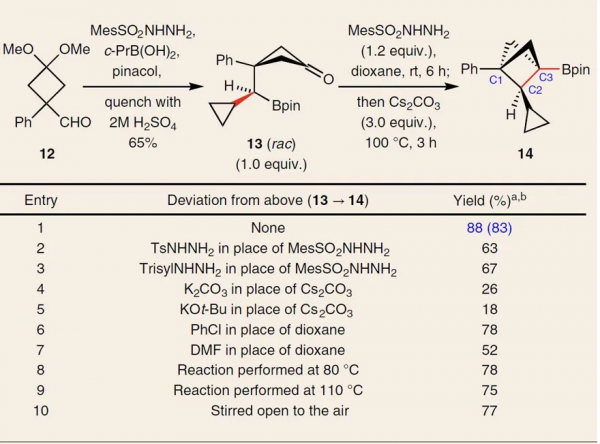
首先,作者從環丁基甲醛12出發,一步法制得關鍵中間體13,隨後13原位形成腙並經先前報道的反應條件,初步實現了橋頭Bpin取代的BCP產物14的合成(圖2,entry 6)。接著,作者對磺醯肼、鹼、溶劑和溫度進行廣泛的篩選後,最終確定了最佳條件:即在均三甲苯磺醯肼為活化劑、碳酸銫為鹼和二惡烷為溶劑的條件下進行反應,能以83%的分離收率獲得偶聯產物14(圖2,entry 1)。值得注意的是,該反應在空氣下就可以順利進行,並不需要惰性氣氛(圖2,entry 10)。
圖2. 條件篩選。圖片來源:Nat. Chem.
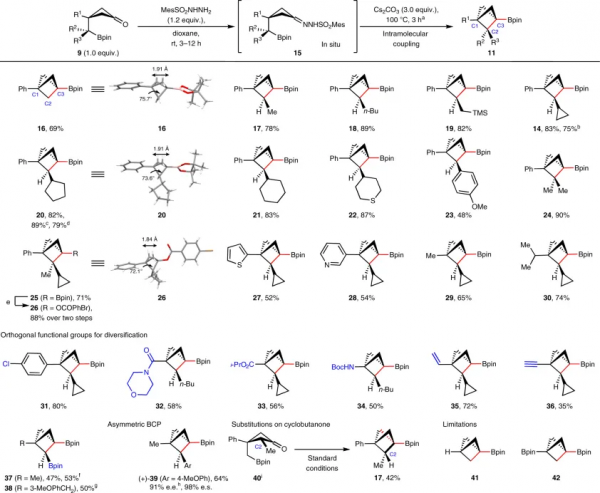
在最優條件下,作者考察了該反應的底物範圍(圖3)。假設環化會受到環丁烷9構象的影響,因此作者選擇位阻較大的苯基(R1=Ph,A值=3.0)取代的環丁烷,對底物的適用性進行了探究,其中A值表示單取代環己烷中平伏取代與軸向取代的構象之比。如圖3所示,伯烷基-Bpin(R2 = H,R3 = H)、仲烷基-Bpins甚至叔烷基-Bpins都能順利地進行環化反應,分別得到C1、C3-二取代BCP-Bpin(16)、C1、C2、C3-三取代BCPs(14和17-23)以及C2位雙取代BCPs(24和25),其中產物14和20還能以克級規模製備。對比BCP 16、20和26的單晶資料,作者發現C2取代基的增加會減小C1-C2-C3之間的夾角,這可能是由於Thorpe-Ingold效應。此外,該反應還能耐受多種官能團,例如:4-氯苯基(31)、2-噻吩基(27)、3-吡啶基(28)、甲基(A值= 1.7,29)、異丙基(A值= 2.1,30)、醯胺(32)、異丙酯(A值=1.2, 33)、乙烯基(A值=1.35, 35)、末端炔烴(A值= 0.41, 36)以及胺(34)等。需要指出的是,C2位-Bpin取代的底物也能相容該反應,以中等的收率得到雙Bpin-取代的BCPs分子(37和38)且能以克級規模進行製備。另外,從手性Bpin前體出發,也能以64%的收率獲得手性BCP 39,並且手性保持不變。除了環丁烷側鏈上的取代基(R2/R3)外,環骨架上C2位-甲基取代的環丁酮40也能以42%的收率轉化為所需的環化產物17。
圖3. 底物拓展。圖片來源:Nat. Chem.
事實上,該策略的戰略性在於能夠將製備的C2-取代BCP-Bpins的模組化(透過交叉偶聯)結合起來,並利用Bpin官能團化實現BCP分子橋頭位置的官能團多樣性(圖4)。例如:1)硼酸酯20可以被氧化為醇43;2)也可以經Aggarwal 芳基化、Zweifel烯化反應和Matteson 同系化構建新的碳碳鍵44、45、46。此外,Bpin 基團也可以轉化為更穩定的三氟硼酸鹽 47,這為進一步官能團化提供了新的機遇。例如:1)47經自由基脫硼可以製備C1,C2-二取代 BCP分子48;2)經鈀催化的Suzuki交叉偶聯反應構建C(sp3)-C(sp2) 鍵49-51;3)原位生成的硼酸與磺醯腙52進行交叉偶聯得到Bpin 53(收率:92%);4)47被BF3•Et2O活化後,能與烷基疊氮化物進行胺化反應,以中等的收率得到胺54-56。此外,化合物57是一種治療失眠的食慾素受體拮抗劑,而且其結構中含有1,3,4-三取代苯環,但之前獲取官能團化BCPs的方法卻不利於製備飽和三取代BCP類似物。相比之下,該方法透過環丙基安裝(59)、環化(33)、Bpin氧化成醇和烷基化(60)等步驟即可快速高效地獲得飽和三取代BCP分子(圖4b),進一步體現了該方法的實用性。
圖4. 合成應用。圖片來源:Nat. Chem.
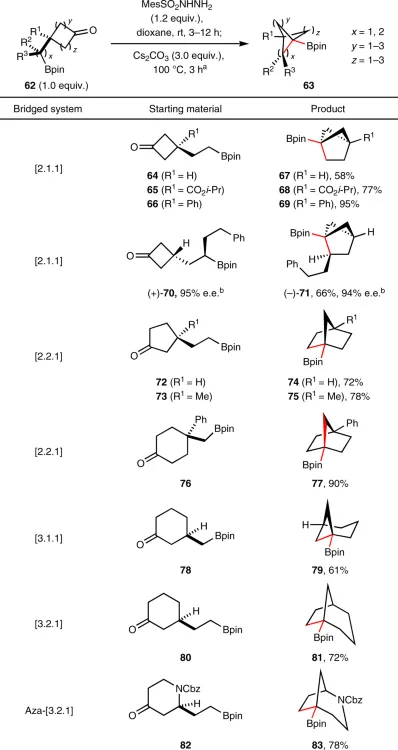
類似地,該策略還能構建其它飽和生物電子等排體的雙環骨架,從而獲得橋頭位置Bpin保留的雙環體系。如圖5所示,從一系列環丁酮(64-66、70)、環戊酮(72和73)、環己酮(76、78和80)以及氮雜環己酮(82)出發,成功地製備了相應的雙環[2.1.1](67-69和71)、[2.2.1](74、75和77)、[3.1.1](79)、[3.2.1](81、83)體系。另外,手性環丁酮-Bpin 70同樣能相容該反應,以良好的收率得到手性[2.1.1]雙環產物71且對映選擇性保持不變,使得有價值的生物電子等排體的不對稱合成成為了可能。
圖5. 雙環系統的構建。圖片來源:Nat. Chem.
總結
秦天教授開發了一種分子內環化反應來製備C1、C2和C3-取代的 BCPs分子。該策略不僅具有操作簡單、化學選擇性好等優勢,而且能夠快速、模組化地製備一系列具有挑戰性的BCP-Bpins分子。此外,該方法已成功製備了一系列目前尚未被完全探索的藥物相關的雙環生物電子等排體。可以預見,該方法將會對藥物研發產生重大影響,特別是在苯替代物的設計和合成等方面。
An intramolecular coupling approach to alkyl bioisosteres for the synthesis of multisubstituted bicycloalkyl boronates
Yangyang Yang, Jet Tsien, Jonathan M. E. Hughes, Byron K. Peters, Rohan R. Merchant, Tian Qin
Nat. Chem., 2021, 13, 950-955, DOI: 10.1038/s41557-021-00786-z
(本文由吡哆醛供稿)