撰文 | Wayne
責編 | 翊竑
微生理系統(MPS),如微流控器官晶片(microfluidic organs-on-chips),已經迅速發展成為有前景的體外工具,其透過重現關鍵的生物過程和疾病狀態來再現人體生理學。然而,它們對藥物開發的價值現在才逐漸清晰。透過結合微系統工程和細胞生物學,MPS建立了可以展示三維結構、多細胞相互作用、組織-組織介面、流體流動和器官層面力學特點的細胞培養模型。例如,它們可以將人類肺部的呼吸力學【1】、透過微血管灌注進行運輸的免疫細胞【2】、微生物群【3】與其他器官進行整合【4, 5】。它們也成為了鑑定潛在疾病治療方法的新工具,包括COVID-19【6】。這些特點使人類多細胞培養系統能夠比傳統的細胞培養更好地複製複雜的組織和器官功能。MPS已經獲得了廣泛的關注,作為一種體外工具,它能夠在病人採用藥物治療之前更好地預測藥物療效和潛在不良反應。
2021年9月17日,瑞士羅氏公司Adrian Roth等研究人員在Science雜誌上發表了題為Human microphysiological systems for drug development的觀點論文,提出器官晶片可用於評估藥物效用並促進個性化醫療。
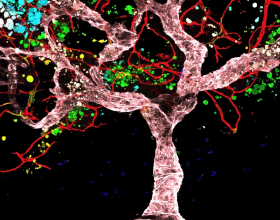
MPS技術可能提供一種方法來更好地理解和解決臨床試驗專案的主要失敗原因——在臨床前的早期階段,動物或較簡單的細胞系統中無法預測療效缺乏或嚴重副作用。MPS提供的關鍵優勢是建立了更多與生理功能相關的人類器官模型(圖1),這些模型可產出藥物作用的資料,並且比動物模型或傳統細胞系統的資料更好地轉化到人類身上。由於不同物種的生理學差異,來自動物的研究資料並不總是能轉化為人類的資料,而傳統的人類體外模型缺乏三維、組織-組織介面和機械因素,這導致了培養細胞的去分化,從而削弱了與體外模型資料與人類生理的相關性。儘管目前的MPS大多處於探索階段,但製藥和生物技術行業對該技術的接受程度很高,其長期目標是最終儘可能地取代動物模型。同時,學術圈和多家生物技術公司都在開發日益完善的MPS模型,用於滿足藥物開發所需的需求和質量標準,包括可擴增性和穩健性。
圖1. 微流控系統可以連線多種型別的人體組織並模仿人類生理學的各個方面,從而改善對藥物反應的評估。
- MPS目前能做什麼?
到目前為止,MPS主要被用於臨床前的安全性(藥物毒理學和代謝),並且一些測試系統已經達到了製藥業內部決策的要求【7】。MPS也被用來解決不同臨床前動物模型之間以及動物和人類之間的差異。例如,大鼠、狗和人的肝臟晶片器官被證明可以重現製藥公司既往在測試中觀察到的特定物種的毒性,同時也為潛在的毒性機制提供新的見解【8】。對於在臨床前動物物種中觀察到的藥效,其是否可轉化應用於人類並不明確,毒性因素可能會促使研發人員選擇次優的候選藥物分子進行進一步開發。因此,人類藥物毒性評估系統可以極大地幫助推動最有希望的候選藥物分子進入臨床。
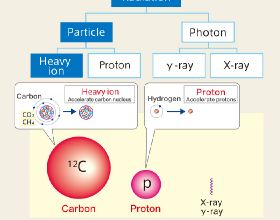
MPS也被用來模擬測試其他的毒性狀況,包括在沒有合適的動物模型或動物模型無法預測人類反應的情況。例如,人類血管晶片再現了導致一種治療性單克隆抗體在人類臨床試驗中失敗的血栓性毒性,而這種毒性在動物的臨床前試驗中從未被發現【9】。一個支援多種血細胞系分化和成熟的血管化人類骨髓晶片也再現了化療藥物和電離輻射暴露後的骨髓紅細胞毒性,以及藥物引起的骨髓功能抑制後的骨髓恢復【10】。此外,由骨組織構成的MPS模型暴露於髖關節植入物相關的鈷和鉻溶解物中,濃度以臨床參考值進行設定,這明確了直接的細胞毒性作用併成功驗證了鉻與松質骨的整合以及與先前在患者中發現的骨間基質鉻結合【11】。
- MPS的新方向是什麼?
儘管解決臨床前安全測試是MPS研究的早期重點,但現在新的研究重心逐漸轉變為療效測試。例如,一個帶有介面內皮的人肺氣道晶片被用來測試抗炎化合物的反應,最近還被用於評估現有和潛在抗病毒療法對SARS-CoV-2感染以及宿主炎症反應的影響【6】。骨髓晶片還被用來模擬一種罕見的遺傳性疾病(Shwachman-Diamond綜合徵),利用從患者身上分離的細胞,這種疾病的關鍵造血缺陷得以重現【10】。透過對患者的細胞進行治療最佳化,這些研究證明了使用MPS開發個性化療法的潛在價值,並有可能協助臨床試驗設計,這對那些非常罕見的疾病患者特別有用,而傳統手段難以系統地進行臨床前藥物測試。
人體複雜的生理過程通常涉及一個以上的器官,因此,MPS的研究人員已經開始建立多器官相互作用的模型,從而更好地研究疾病生物學或藥物作用。例如,多器官MPS應用於研究神經活性藥物,如甲基苯丙胺,探究其如何穿過血腦屏障並對大腦的神經元產生影響【12】。由相連的人類肝臟、腎臟和腸道器官晶片所組成的第一道藥代動力學模型與計算模型相結合,用於定量預測藥物的藥代動力學和藥效學特徵【4】。連線腸道、肝臟、大腦和腎臟的整合型MPS模型使用來自單一捐贈者的誘導多能幹細胞進行分化【13】,這可能在未來實現供體特異性的個體化多器官研究和藥物測試。如果與患者來源的幹細胞或類器官方法相結合【14】,這種模型可以在患者個體層面提供量身定做的精準醫療工具。
與常用的免疫缺陷或半人源化的動物模型不同,人類MPS適用於腫瘤的移植【15】和微生物病原體的感染【6】,並且對人類特異性病毒具有特別的優勢。然而,由於缺乏對這一新興技術的充分驗證和經驗,迄今為止,沒有一個MPS檢測方法被用作藥物審批【7】。因此,如何從研究級的MPS檢測方法躍升為經驗證的可靠藥物開發工具,併產生符合監管部門審查要求的結果是當前研究的重要挑戰。由於藥物開發越來越注重開發高度工程化的治療分子,而這些分子在任何動物模型中都不會與目標發生交叉反應,因此除了使用人類體外模型,往往沒有其他選擇。由於供應短缺,使用非人靈長類動物進行藥物和疫苗測試也變得更加困難(例如COVID-19的疫苗測試),此外還有隨之而來的倫理問題。因此,現在比以往任何時候都更需要用人類細胞來替代臨床前模型的體外試驗。
- 總結
MPS還可以推動新的療法快速發展,以滿足緊迫的醫療需求,例如,針對大流行病毒的信使RNA(mRNA)疫苗或嵌合抗原受體(CAR)T細胞癌症免疫療法。儘管這些療法經傳統方法驗證獲得批准,但對這種創新的藥物模式往往需要進行批准後的跟蹤研究,進而擴大安全和療效資料庫。MPS模型具有較大的潛在價值,如果將這種晶片模型上獲取的資料與真實世界資料一起聯合分析,能夠建立一個更為準確的模型用於預測。透過將相關監管部門的建議納入晶片試驗(on-chip trial)的設計,這種方法的成功性將得到進一步加強。例如,可以使用美國食品和藥物管理局(US FDA)的藥物開發工具資格認證程式,就像用於驗證生物標誌物一樣,將MPS的開發作為新藥創新科技方法(ISTAND)試點計劃的一部分(該計劃旨在促進藥物研發中新方法的開發)。結合先進的資料分析、計算機建模和模擬,每次針對一個特定情景(如一種特定的疾病和治療方式)進行反覆探索,MPS最終可以為監管機構提供可用的資料集,其預測能力可能比以前用動物模型生成的資料集要高。一旦某個案例的概念性驗證得以成功,其他的解決方案也會隨之而來。
本文來自BioArtMED微信公眾號,更多生物領域前沿資訊等你來發現!
轉載須知
【原創文章】BioArtMED原創文章,歡迎個人轉發分享,未經允許禁止轉載,所刊登的所有作品的著作權均為BioArtMED所擁有。BioArtMED保留所有法定權利,違者必究。