來源:煙臺日報-大小新聞
綠葉製藥集團宣佈,其控股子公司博安生物自主開發的度拉糖肽注射液(BA5101)已獲得中國國家藥品監督管理局藥品審評中心批准開展臨床試驗。博安生物致力於構建具有差異化的多樣性產品組合,涵蓋生物類似藥、創新抗體、細胞治療等領域,其各類管線的研發程序正在密集推進中。
BA5101是一種新型長效胰高血糖素樣肽-1(GLP-1)受體激動劑,每週給藥一次,為Trulicity(度易達)的生物類似藥,用於治療成人2型糖尿病。
與其他降糖藥相比,度拉糖肽注射液能夠促進胰島素分泌、抑制胰高血糖素分泌、改善胰島β細胞的功能,有效降低血糖及糖化血紅蛋白(HbA1c)水平,且獨特的作用機制使其更不易引起低血糖,同時能改善體重、血脂等多個心血管疾病的危險因素,具有獨特的臨床優勢。不僅如此,已有多項臨床研究表明:作為一種安全有效的長效治療2型糖尿病藥物,度拉糖肽注射液每週一次的給藥方式可降低患者用藥時產生的抵抗心理及不便,提高依從性,改善其生活質量。
BA5101的臨床前研究顯示:該產品在藥學、藥代動力學及毒理學方面與度易達具有高度相似性。目前,博安生物正在積極推進BA5101的研發程序並計劃在全球其他國家和地區開展該藥物的註冊工作。
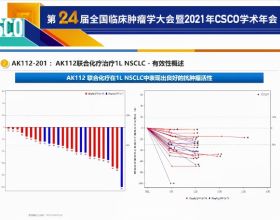
無論在中國還是全球範圍內,糖尿病的防控形勢異常嚴峻。國際糖尿病聯盟(IDF)資料顯示:截至2019年,全球約有4.63億20-79歲成人患有糖尿病,預計到2045年病患總數將增至7億1。作為糖尿病大國,我國18歲及以上人群的糖尿病患病率則高達11.2%2。 鑑於該疾病領域大量未滿足的患者需求,度拉糖肽注射液在全球範圍呈現廣闊的市場前景。2014年,Trulicity率先在美國獲批,此後在歐盟、日本、中國等多個國家和地區上市。該產品在全球範圍內獲批的適應症包括:(1)適用於成人2型糖尿病的血糖控制;(2)用於降低伴有心血管疾病或具有多重心血管風險因子的成人2型糖尿病患者的主要心血管事件風險。公開的財務報告顯示:Trulicity2020年的全球銷售額達到50.7億美元,同比年增長率為23%。
博安生物研發總裁兼營運長竇昌林博士表示:度拉糖肽注射液的研發,是滿足患者臨床需求的重要途徑。透過開發高品質、可負擔的生物藥治療方案,我們希望積極提升全球糖尿病患者的用藥可及性。
除了BA5101,博安生物已透過高效的自主創新能力,成功開發出多樣化的在研創新生物藥和生物類似藥,並在細胞治療等前沿技術領域積極佈局;其研發管線包含10多個擁有國際智慧財產權保護的創新抗體以及一系列生物類似藥的產品組合。作為集團轉型升級的重要業務領域之一,綠葉製藥不斷加大投入,透過博安生物加速推動其生物藥的全球戰略佈局。
責編:李志娟
本文來自【煙臺日報-大小新聞】,僅代表作者觀點。全國黨媒資訊公共平臺提供資訊釋出傳播服務。
ID:jrtt