乙肝病毒慢性感染全球超過2.4億人,可導致慢性肝炎、LC和HCC。最近一年來,CRISPR/Cas9技術被科學家提及,有望成為直接破壞HBV基因組的一種新療法。由於HBV基因組序列的高度多樣化,異質患者的目標HBVDNA中,不一定完整地存在長度為20個核苷酸的嚮導RNA(gRNA)的相同靶序列。
乙肝CRISPR/Cas9,提供多個基因敲除,解決異質靶點及逃避突變體
一、腺病毒載體可穩定維持八個多重gRNA表達
因為上述原因,可行的基因組編輯藥物,還僅僅只對有限數量的患者有效。日本四所科研院校研究人員在International Journal of Molecular Sciences上,介紹了透過CRISPR/Cas9表達的八種多重引導RNA的腺病毒載體,能夠有效破壞來自異質患者的多種乙肝病毒基因,這是最近基於乙肝研究領域應用CRISPR/Cas9技術的比較前沿的進展!
在這項研究中,研究人員發現腺病毒載體 (AdV)基因組中,穩定地維持了八個多重 gRNA表達單元。使用該 AdV表明,存在於來自異質患者的細胞染色體中的HBV X DNA可以在四個或五個預期位點同時切割,併產生不可逆的缺失。
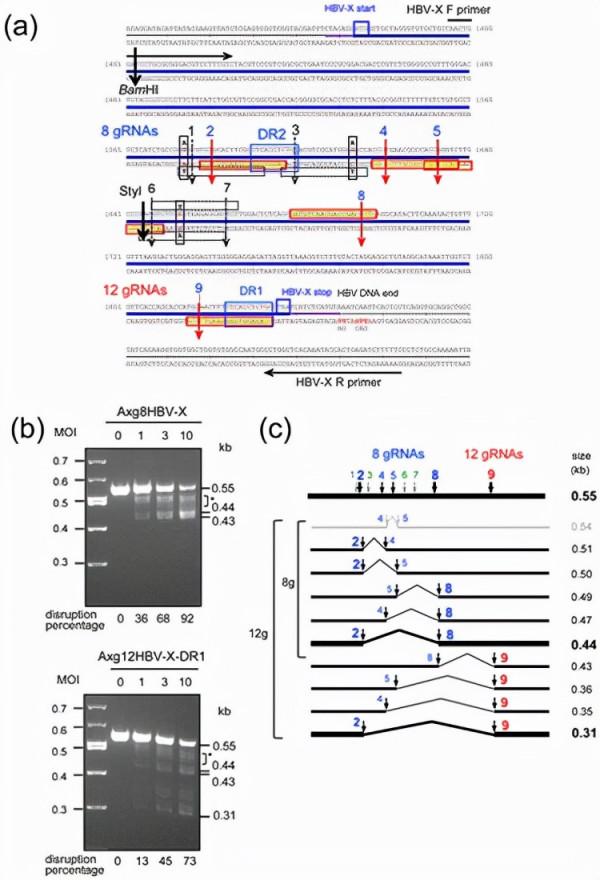
來自:International Journal of Molecular Sciences,使用表達 8 和 12 gRNA 的 AdV 破壞來自不同患者的 HBV X 基因
二、解決以往技術問題
結果表明,儘管HBVDNA序列高度多樣化,但當在HBVDNA整合位點切割細胞染色體有效時,單個 AdV可用作基因組編輯治療的可能的抗HCC藥物。同樣的AdV也可用於治療慢性或急性乙肝。雖然報告的AdV包含8個gRNA單位,但這個數字遠大於使用其他病毒載體的數量:已經報告了使用慢病毒、AAV和腺病毒載體的四種多重gRNA。
此前,全球只有報道過四種gRNA,而本研究的AdV可同時表達八種多重gRNA。多重gRNA表達,使我們能夠使用Cas9切口酶的雙切口策略,將脫靶效應降低多達1500倍。這種策略提供了更安全的基因組編輯療法,適用於所有使用CRISPR/Cas9 系統的實驗。
雙切口策略,以往主要面臨的一個問題是一次切割的兩個gRNA都必須是有活性的,因此切割效率低的可能性增加。同時,在實驗前測定所有候選gRNA的活性也就不切實際,並且可能存在影響gRNA活性的位置效應。因此,對單個目標使用兩個雙切口是安全的。
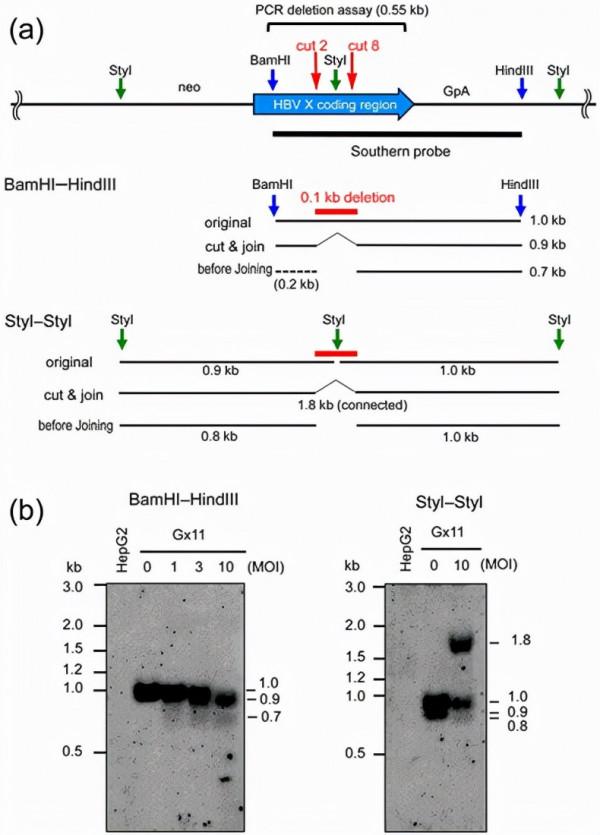
整合到Gx11細胞染色體中的 HBV X 基因的Southern分析,被表達8個gRNA單位的AdV破壞
三、AdV相比以往更有優勢
此外,如果可能,敲除一個基因的兩個位點或同時破壞兩個基因可以有效地使級聯功能失活。出於這些原因,八單元AdV是可取的。在本研究中,表達八個多重gRNA的AdV顯然更具有優勢!將此策略與AAV載體一起使用是有困難的,因為saCas9的基本PAM序列NNGRRT 的頻率低於 spCas9、NGG。
在由HBV引起的HCC中,多個整合的病毒DNA通常存在於同一細胞的單個或多個染色體中。如果在一條染色體中至少存在兩個靶標,並且即使病毒DNA序列中存在兩個靶點,那麼使用多重gRNA方法,一條染色體中兩個病毒DNA之間的大量缺失或產生的兩條或更多條染色體的損傷,可能會影響這些HCC細胞的生存能力。
四、未來開發前景
小番健康結語:研究人員描述了這樣一項研究結論,表達八種多重gRNA的AdV是穩定的,儘管有必要檢查這些AdV是否可以穩定地放大到足以用於治療目的的規模,但它們可以應用於HBV HCC和慢性肝炎的基因組編輯療法。它們也可能對需要同時敲除多個基因的基礎研究有用。
近一年來,越來越多和CRISPR/Cas9相關研究被研究人員發表,且已有一些針對特定疾病的基因編輯藥物進入臨床研究。過往對基因組編輯應用於慢性乙肝的研究發現,它僅對有限的患者有效。研究人員最近開發的這種可以一步構建帶有八個多重gRNA表達單元的腺病毒載體(AdV),使用它,可以切割並破壞來自異質患者整合的 HepG2 細胞染色體中的HBV X基因的多個位點!
由於序列不匹配,八個靶點中有四個不能被切割,但其餘四個靶點被切割,併產生不可逆的缺失。因此,多樣化的X基因被破壞效率超過90%。含有八個多重gRNA單元的AdV,不僅可以提供多個基因敲除,而且還可以解決基因組編輯治療中異質靶點和逃避突變體的問題。
祝朋友們國慶節日快樂!