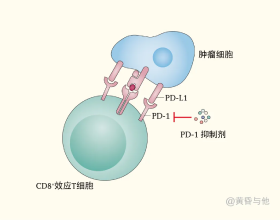
腦部腫瘤具有獨特的生理特徵,其內部充滿了髓系細胞並有血腦屏障,具有和機體其他器官顯著不同的免疫環境[1,2]。目前,腦腫瘤逃避免疫抑制的具體機制還不清楚。儘管免疫檢查點阻斷CD8+T細胞對很多腫瘤都有療效,但是腦腫瘤幾乎沒有免疫應答[3]。浸潤的CD8+T細胞增加通常預示著更好的預後,但在腦瘤中CD8 T細胞的浸潤和病人生存期沒有關係[4,5],可能是因為腦瘤中有獨特的免疫抑制機制。
腫瘤細胞能夠逃逸免疫監視有很多原因,其中腫瘤細胞內氧代謝是影響腫瘤免疫抑制的重要因素。腫瘤細胞的過量呼吸導致微環境低氧,降低抗腫瘤免疫[6,7]。低氧影響多種免疫細胞的功能,比如低氧干擾了自然殺傷細胞(NK細胞)的毒性以及機體招募CD8 T細胞到腫瘤區域的能力[8],低氧腫瘤相關巨噬細胞抑制T細胞應答,促進腫瘤生長和血管新生[9]。儘管低氧是腦瘤的顯著特徵,但是低氧影響腫瘤免疫的機制尚不清楚,低氧狀態下γδ T的功能也有待揭示。在人類腦瘤中,γδ T細胞是執行固有免疫的一類T細胞,佔有所有T淋巴細胞的0.5%-5%。γδ T細胞具有細胞毒性,可以浸潤到腦瘤區域,在體內體外實驗中都發現γδ T細胞可以抵抗腦瘤[10],但是在小鼠模型中,γδ T細胞缺失並不影響腦腫瘤生長。
2021年3月22日,來自韓國科學技術院(KAIST)的 Heung Kyu Lee教授團隊在《自然·免疫學》雜誌發表論文,解析了腫瘤細胞和免疫細胞尤其是γδ T細胞相互作用的重要機制,強調了γδ T細胞在腦腫瘤免疫中的臨床重要性。
透過對TCGA和CGGA兩個資料庫分析發現CD4和CD8 T細胞浸潤和腦腫瘤患者的生存期負相關,CGGA資料庫顯示γδ T細胞浸潤和腦腫瘤患者,尤其是低級別的腦瘤患者的生存期正相關。研究人員透過基因敲除系統建立了高級別膠質瘤(HGG)小鼠模型,發現CD4 T細胞浸潤增加,而CD8 T細胞和γδ T細胞減少,提示腫瘤微環境抑制了γδ T細胞的浸潤。
為了研究淋巴細胞對腦癌的影響,研究人員在GL261(小鼠膠質瘤細胞)原位HGG模型中去除了各種型別的淋巴細胞,發現CD8和CD4 T細胞的缺失以及自然殺傷細胞和γδT細胞的缺失均不影響HGG小鼠的總體存活率。這些資料提示在腦腫瘤中淋巴細胞被抑制,喪失了抗腫瘤功能。
那麼腫瘤浸潤的γδ T細胞有哪些功能呢?對原位HGG中腫瘤浸潤的淋巴細胞的單細胞測序分析顯示腫瘤中γδ T細胞處於低氧狀態且Bax(BCL2-Associated X,促凋亡基因)表達量較高。根據CGGA資料庫分析,HIF1α的表達會隨著腫瘤級別的增加而增強,而γδ T細胞浸潤和HIF1α以及BAX的表達負相關,這些資料說明腦腫瘤浸潤的γδ T細胞處於低氧狀態,且其凋亡訊號通路被啟用,從而抑制了γδ T細胞的抗腫瘤功能。
對不同型別的腫瘤細胞進行耗氧率檢測發現腦腫瘤細胞耗氧率最高。使用二甲雙胍抑制線粒體複合體I的功能,發現二甲雙胍對腫瘤細胞的影響顯著高於對淋巴細胞的影響。二甲雙胍降低了GL261細胞的耗氧率,不影響其糖酵解。小鼠體內實驗發現二甲雙胍處理緩解了腫瘤細胞微環境的低氧狀態,因此二甲雙胍在體內和體外都有抗低氧的功能,二甲雙胍處理使腫瘤體積減小,HGG原位瘤小鼠生存期延長,這些資料表明:在腦腫瘤中,二甲雙胍透過緩解腫瘤微環境中的低氧狀態產生抗腫瘤的功效。因此,緩解腦腫瘤中的低氧狀態具有抗腫瘤效果。
那麼二甲雙胍的抗腫瘤功效是否和T細胞的功能相關呢?透過T細胞缺失的裸鼠實驗發現去除T細胞後,二甲雙胍的抗腫瘤效果消失。敲除CD4和CD8 T細胞不影響二甲雙胍的抗腫瘤效果,而敲除γδ T 和Tcrd嚴重降低了二甲雙胍的抗腫瘤效果,說明γδ T細胞介導了二甲雙胍的抗腫瘤效果。二甲雙胍處理增強了γδ T細胞的浸潤,但對CD4和CD8 T細胞無顯著影響。因此二甲雙胍透過γδ T細胞發揮抗腫瘤作用,不依賴於傳統T細胞。
為了調查二甲雙胍對γδ T細胞的轉錄水平的影響,研究人員對二甲雙胍處理的小鼠和對照組做了單細胞RNA測序,發現二甲雙胍處理的小鼠有一個γδ T細胞亞群的抗腫瘤活性最強。γδ T需要NKG2D受體和T細胞受體(TCR)來產生細胞毒性。二甲雙胍處理的腫瘤細胞高表達顆粒酶B(Gzmb)和γ干擾素(IFN-γ),並且缺氧誘導因子-1α(Hif1α)和Bax表達降低。二甲雙胍處理抑制了腫瘤細胞呼吸,緩解了腫瘤微環境中的低氧狀態,使腫瘤細胞中的HIF1α表達降低、T細胞凋亡減少、γδ T細胞呼吸增強,細胞的整體先天免疫應答增強。因此增強γδ T細胞活性可以減緩腦腫瘤生長。
二甲雙胍處理使CD27+ CD44int γδ T細胞(即IFN-γ的γδT細胞)數量增加,PD-1表達降低,多種細胞因子共同免疫作用增強,二甲雙胍處理的小鼠腫瘤組織中的IFN-γ濃度比對照組中濃度高。二甲雙胍介導的氧氣增加激活了γδ T抗腫瘤免疫應答。GL261細胞表達NKG2D的配體Rae-1, 二甲雙胍處理增強了γδ T細胞中的NKG2D的表達,NKG2D陽性的γδ T細胞可以產生IFN-γ,殺傷腫瘤細胞。因此復氧條件下,二甲雙胍處理可以啟用γδ T細胞,恢復其免疫殺傷功能。
那麼腫瘤的低氧環境如何調控γδ T細胞中NKG2D的表達呢?使用線粒體複合體I抑制劑魚藤酮(Rotenone)處理細胞模擬低氧環境,Rotenone處理降低了γδ T細胞中NKG2D的表達。在線蟲中低氧透過cAMP通路啟用PKA訊號通路,單細胞測序分析發現腫瘤浸潤的γδ T細胞PKA表達較高,進一步研究發現低氧在轉錄水平調節了PKA的表達。使用cAMP的類似物Sp-8-Br-cAMP處理細胞可以抑制γδ T細胞中NKG2D的表達。Rotenone的處理促進了γδ T細胞中PKA亞基的表達,而二甲雙胍處理降低了體內PKA的表達。因此 二甲雙胍介導的腫瘤微環境中復氧透過cAMP-PKA軸調控γδ T細胞中NKG2D的表達。NKG2D表達升高提高了γδ T細胞的敏感性,使其產生抗腫瘤的細胞因子,對腦腫瘤微環境中的腫瘤細胞具有直接細胞毒性。
(圖片引自“風溼中心”http://www.360doc.com/content/21/0417/09/72388143_972734842.shtml)
綜上所述,本文揭示了一個低氧介導的免疫細胞抗腫瘤機制,強調了γδ T細胞在腫瘤免疫中的重要作用。腦腫瘤細胞的氧濃度和免疫細胞功能密切相關,γδ T細胞需要NKG2D產生干擾素,而低氧透過啟用PKA訊號通路抑制γδ T細胞中NKG2D的表達從而抑制γδ T細胞的腫瘤殺傷功能。二甲雙胍處理降低了γδ T細胞中PKA亞基的表達,增強了NKG2D的表達從而恢復了γδ T細胞的免疫功能。二甲雙胍處理與抑制HIF-1α聯合療法可以提高γδ T的抗腫瘤作用,本文為腦瘤的免疫治療提供了一種新的臨床治療思路。
參考文獻
[1] Thorsson, V. et al. The Immune Landscape of Cancer. Immunity 48, 812-+, doi:10.1016/j.immuni.2018.03.023 (2018).
[2] Arvanitis, C. D., Ferraro, G. B. & Jain, R. K. The blood-brain barrier and blood-tumour barrier in brain tumours and metastases. Nat Rev Cancer 20, 26-41, doi:10.1038/s41568-019-0205-x (2020).
[3] Lim, M., Xia, Y., Bettegowda, C. & Weller, M. Current state of immunotherapy for glioblastoma. Nat Rev Clin Oncol 15, 422-442, doi:10.1038/s41571-018-0003-5 (2018).
[4] Barnes, T. A. & Amir, E. HYPE or HOPE: the prognostic value of infiltrating immune cells in cancer. Br J Cancer 117, 451-460, doi:10.1038/bjc.2017.220 (2017).
[5] Zhai, L. et al. IDO1 in cancer: a Gemini of immune checkpoints. Cell Mol Immunol 15, 447-457, doi:10.1038/cmi.2017.143 (2018).
[6] Rivadeneira, D. B. & Delgoffe, G. M. Antitumor T-cell Reconditioning: Improving Metabolic Fitness for Optimal Cancer Immunotherapy. Clin Cancer Res 24, 2473-2481, doi:10.1158/1078-0432.CCR-17-0894 (2018).
[7] Scharping, N. E. & Delgoffe, G. M. Tumor Microenvironment Metabolism: A New Checkpoint for Anti-Tumor Immunity. Vaccines (Basel) 4, doi:10.3390/vaccines4040046 (2016).
[8] Zheng, X. et al. Mitochondrial fragmentation limits NK cell-based tumor immunosurveillance. Nat Immunol 20, 1656-1667, doi:10.1038/s41590-019-0511-1 (2019).
[9] Henze, A. T. & Mazzone, M. The impact of hypoxia on tumor-associated macrophages. J Clin Invest 126, 3672-3679, doi:10.1172/JCI84427 (2016).
[10] Bryant, N. L. et al. Preclinical evaluation of ex vivo expanded/activated gammadelta T cells for immunotherapy of glioblastoma multiforme. J Neurooncol 101, 179-188, doi:10.1007/s11060-010-0245-2 (2011).