胃癌,一個聽起來讓我們感到熟悉又害怕的病症。我們熟悉是因為它在我國的發病率較高,而害怕的原因在於它位列全球範圍內癌症死因的第四位[1]。對於這樣的疾病,怎樣的治療方案最有效呢?
前不久,來自日本國立癌症研究中心東醫院的Kohei Shitara教授領銜全球多個研究團隊在《柳葉刀》雜誌公佈了一項名為CheckMate 649的III期臨床研究結果[2],讓晚期胃癌的免疫治療終見光明!
研究結果表明:與單獨化療相比,PD-1抑制劑納武利尤單抗聯合化學療法,將患者的中位總生存時間延長了3.3個月。換句話說,納武利尤單抗聯合化療將患者的死亡風險降低了29%。
現階段,針對HER2陰性的晚期/轉移性胃癌(GC)/胃食管結合部癌(GEJC)/食管腺癌(EAC)患者,基於氟尿嘧啶和鉑類聯合使用的一線化療用藥,治療效果依舊不理想,中位總生存期(OS)不足一年[3]。雖然有一些其他靶向藥物不斷推陳出新,但依舊無法顯著延長患者的生存期[4]。
讓人眼前一亮的是:在III期ATTRACTION-2研究中,PD-1抑制劑納武利尤單抗(Nivolumab,NIVO)較安慰劑組,可以為既往接受過兩種及以上化療方案的GC/GEJC患者,帶來顯著生存獲益[5]。
因此研究者基於免疫檢查點療法在GC/GEJC疾病模型上展開了大量臨床試驗,如ATTRACTION-4(一線治療)、KEYNOTE-062(一線治療)、KEYNOTE-590(一線治療)、JAVELIN Gastric 100(化療誘導後的二線治療)等。

經總結髮現,本被寄予厚望的針對晚期胃癌的一線化療聯合免疫治療,僅KEYNOTE-590在亞層分析中,基於特定疾病模型,可以提高PFS/OS[2]。
那麼化療聯合免疫治療是否可以真正造福未經治療的晚期胃癌患者呢?
為進一步確證納武利尤單抗在GC/GEJC患者一線治療中的有效性,研究者開展了一項名為CheckMate 649的III期臨床試驗,旨在評估與單獨化療相比,納武利尤單抗(NIVO)聯合化療用於晚期未經治療GC/GEJC/EAC患者的治療效果。
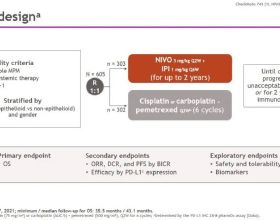
CheckMate 649是一項全球範圍、隨機、多中心、開放標籤的臨床研究,在29個國家的175家醫院和癌症中心有序開展。其入組標準和具體的試驗方案如下圖所示:
接下來,我們就一起來看看本研究的主要結果。
首先,基於主要終點分析,對於PD-L1 CPS≥5的患者,從中位總生存時間(OS)來看,單獨化療組患者是11.1個月,NIVO聯合化療組是14.4個月,聯合治療組患者的中位總生存時間延長了3.3個月。也就是說,NIVO聯合化療將患者的死亡風險降低了29%(HR 0.71,P<0.0001)。
從中位無進展生存期(PFS)來看,單獨化療組患者是6.0個月,NIVO聯合化療組是7.7個月,聯合治療將患者的疾病進展風險降低了32%(HR 0.68,P<0.0001)。
之後,基於次要終點分析,對於PD-L1 CPS≥1的患者,從中位總生存時間(OS)來看,單獨化療組患者是11.3個月,NIVO聯合化療組是14.0個月,NIVO聯合化療將患者的死亡風險降低了23%(HR 0.77,P<0.0001);從中位無進展生存期(PFS)來看,單獨化療組患者是6.9個月,NIVO聯合化療組是7.5個月。
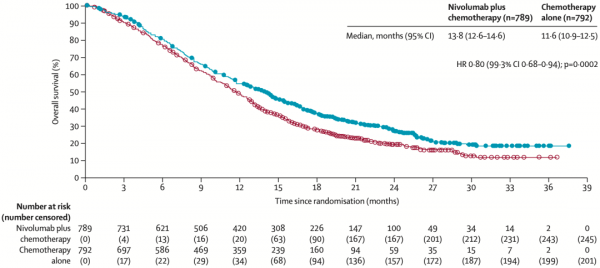
對於所有患者,從中位總生存時間(OS)來看,單獨化療組患者是11.6個月,NIVO聯合化療組是13.8個月,NIVO聯合化療將患者的死亡風險降低了20%(HR 0.80,P=0.0002)。從中位無進展生存期(PFS)來看,單獨化療組患者是6.9個月,NIVO聯合化療組是7.7個月,表明所有患者均有PFS獲益。
至於NIVO聯合化療的安全性,在聯合治療和單獨治療中,最常見的不良反應均為噁心、腹瀉和周圍神經病變。
對於3-4級治療相關的不良反應,NIVO聯合化療組在782名患者中有462名患者(59%),單獨化療組在767名患者中有341名患者(44%)。雖然NIVO聯合化療組不良反應人數較多,但這其中與免疫相關的不良反應是少於5%的,未觀察到新的不良反應訊號。因此整體來說聯合治療的安全性是可以接受的,是在可控範圍內的。
基於CheckMate 649這一大規模的臨床研究結果,FDA已批准納武利尤單抗聯合氟尿嘧啶和鉑類藥物用於治療晚期或轉移性GC/GEJC/EAC的患者。
這一研究成功,可能來源於多方面因素。首先,對於胃癌,已有研究證明納武利尤單抗在GC/GEJC/EAC治療中的有效性;其次是化療與免疫治療的有效結合,化療藥物不僅可以發揮殺傷作用,同時可以透過免疫原性死亡效應增強免疫反應[6];更重要的一點是設定了兩種化療給藥方案,並考慮了聯合治療的耐受性,及不同患者的差異性和順應性等問題,從而可以更好的個性化治療。
這一臨床試驗結果,不僅打消了臨床對於胃癌免疫治療的爭議與猶豫,可以讓更多的晚期胃癌患者從中獲益,獲得長期高質量的生存,有望改變胃癌一線治療的格局;同時為免疫治療聯合化療的科學研究注入一劑強心針,可以鼓舞更多的研究者,今後努力探索聯合免疫治療的新思路。
[1] Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021;71(3):209-249. doi:10.3322/caac.21660
[2] Janjigian YY, Shitara K, Moehler M, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial [published online ahead of print, 2021 Jun 4]. Lancet. 2021;S0140-6736(21)00797-2. doi:10.1016/S0140-6736(21)00797-2
[3] National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines). Gastric cancer. Version 2. 2021. https://www.nccn.org/professionals/physician_gls/ pdf/gastric.pdf (accessed March 17, 2021).
[4] Shah MA, Bang YJ, Lordick F, et al. Effect of Fluorouracil, Leucovorin, and Oxaliplatin With or Without Onartuzumab in HER2-Negative, MET-Positive Gastroesophageal Adenocarcinoma: The METGastric Randomized Clinical Trial. JAMA Oncol. 2017;3(5):620-627. doi:10.1001/jamaoncol.2016.5580
[5] Kang YK, Boku N, Satoh T, et al. Nivolumab in patients with advanced gastric or gastro-oesophageal junction cancer refractory to, or intolerant of, at least two previous chemotherapy regimens (ONO-4538-12, ATTRACTION-2): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2017;390(10111):2461-2471. doi:10.1016/S0140-6736(17)31827-5
[6] Park SJ, Ye W, Xiao R, et al. Cisplatin and oxaliplatin induce similar immunogenic changes in preclinical models of head and neck cancer. Oral Oncol. 2019;95:127-135. doi:10.1016/j.oraloncology.2019.06.016