這或許是新的財富入口
9月23日,華為公佈了華為雲盤古藥物分子大模型。這套模型專門面向藥物研發,據官宣:已經學習了17億個藥物分子的化學結構,並生成了1億個創新的類藥物小分子,能實現從靶點計算匹配到後續定向最佳化的全部過程。
17億、1億……典型的網際網路企業計數量級。
就在傳統藥企還在糾結PD-1、EGFR等熱門靶點時,計算機和人工智慧已經開始瞄準多達80%的“不可成藥靶點”,試圖開發藥物。
製藥工業上百年,如今,有人要用新技術,去碰撞傳統的“不可成藥”問題。
DEL,給出上千億個化學結構
2020年9月25日,四川地區上市公司組織投資者集體網上接待日活動,有投資人問:
“藥明康德進入DEL技術領域,會不會加劇市場競爭?”
DEL,全稱是DNA編碼化合庫,該技術最早由美國Scripps研究院的Sydney Brenner和 Richard Lerner 於1992年提出,旨在提高靶點篩選效率,被視為發現小分子藥物的有效篩選技術之一。
其基本原理是用DNA片段對每種化合物進行編碼,之後化合物不斷排列組合,再得到新的化合物。10個分子,兩兩結合一次便會產生100個新分子,結合第二次就生成10000個……如此反覆,DEL化合物庫內可含有千億級結構新穎的小分子。
在結合過程中,DNA片段始終定位著基礎化合物的位置。如果將DEL視為圖書館,小分子是其中的書籍,DNA片段便是書籍的唯一標識。
研究者可透過小分子所帶的DNA片段,對其進行識別、二次試驗,找出對靶點蛋白髮揮作用的小分子。
基於這樣的原理,DEL技術被認為可以幫助藥企找到成藥性高的新穎分子。這樣的苗頭,CRO巨頭自然不會放過。目前,藥明康德已經推出了DELopen和DELlight平臺,康龍化成、藥石科技和美迪西也在DEL領域均有佈局。
在萬物皆可AI的時代,AI並非只為醫藥研發而來。在AI之外,DEL同樣值得關注:AI製藥的最大前提是有一個龐大的化合物資料庫,DEL技術正好提供了海量的化學結構。
所以說,未來的藥物開發,完全可能有另外一套模式。
無用的創新?
DEL火熱的另一面,是常規新藥研發成本不斷上漲,成功率卻在下滑。
2014年,美國塔夫茨藥物開發研究中心曾釋出報告:一款新藥從研發至上市平均需要耗費26億美元,不再是行業普遍認為的“10億美元”數量級。2019年,IQVIA釋出報告顯示,2018年全球新藥研發的成功率僅為11.4%。
研發效率不高的情況下,葛蘭素史克最先看到DEL潛力。2007年,GSK花費5500萬美元的價格,收購了DEL技術先鋒公司Praecis,帶領了DEL技術產業的起跑;2014年3月到2016年6月,全球共有19個活性分子來源於DEL技術,其中GSK佔了12個。
GSK之後,全球排名前20的藥企幾乎全部佈局了DEL技術。
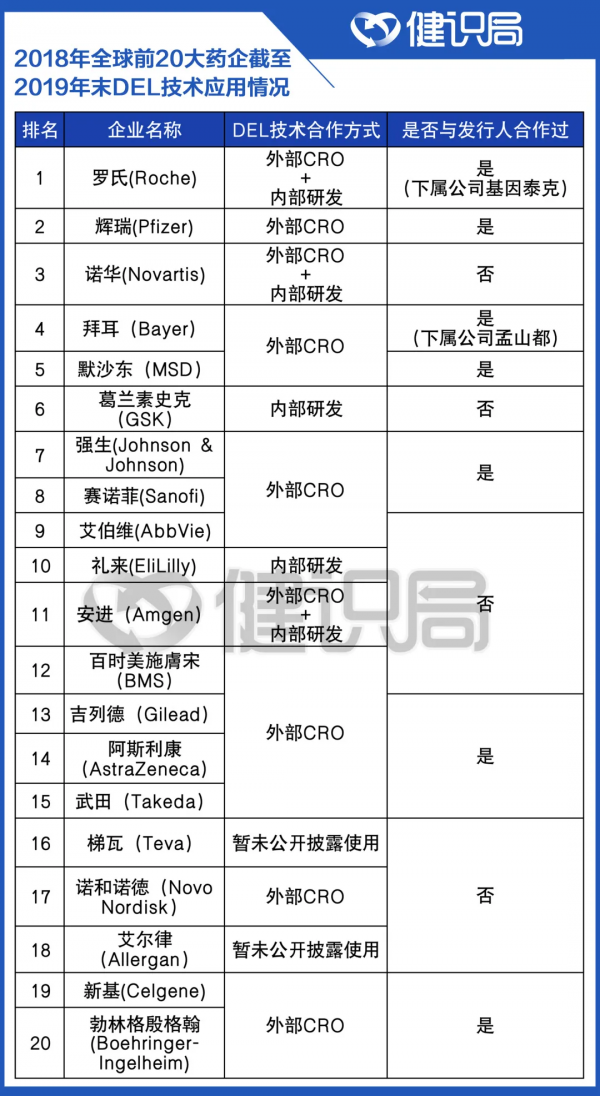
根據X-Chem公司官網、Nuevolution招股書、年報及公開資料整理
新事物有魅力,在於其帶著未知的誘惑。但是,能否真正推動時代、顛覆過往,需要有力的自我證明。
截至目前,還未有新藥透過DEL技術發現並且上市。即便是GSK,旗下相關藥物的最快進度也不過處於臨床Ⅱ期。
透過DEL技術篩選,的確能夠得到有靶點親和力的小分子,“這仍是很前期的研究,這些反應也可能是假陽性,真正要走到成藥分子並不容易。”業內人士告訴健識局。
統計資料也證明了這一點。在新藥研發的小分子篩選中,主要的篩選方式是已知活性化合物、傳統高通量篩選(傳統HTS)、基於結構的藥物設計(SBDD)、定向篩選、基於分子片段的藥物設計(FBLG)等多種方式。據2016年-2017年發表在《J.Med.Chem》的分析資料,實際開發中,上述藥物篩選方法使用的比例約為30%、29%、14%、8%和5%。
而使用DEL技術進行藥物篩選的比例,僅為1%。
上述人士表示:DEL技術的最大意義是吸引更多研究者參與,才有機會篩出合適的分子。
目前,國內基於DEL技術進行藥物早期研發代表企業之一是成都先導,該公司的DEL庫中,有超過4000億個化學結構。即使是入局不久的華為盤古云AI模型,也已學習了17億個化學結構。
DEL技術給製藥業出了個難題:給了無窮多的可能,然後讓你大海撈針。
DEL的新戰場
目前,DEL技術仍處在非主流階段,稚嫩背後,是DEL難以逃脫的侷限性。
侷限之一,是應用場景有限。核酸具有水溶性,這也就意味著含有DNA的DEL反應需要在水中或水溶劑中進行;同時,為了保護DNA編碼的資訊完整,DEL反應的環境又不能太極端。
但是,不是所有化合反應都能在這樣的“舒適條件”下完成,因而,DEL技術組合出來的分子種類規模有限。
侷限之二,是DEL應用於靶點篩選的時候,只能針對純化的生物靶點發揮作用;遇到可對DNA分子本身反應或降解的靶點時,DEL技術的穩定性便會受到干擾。
侷限之三,DEL不是傳統的單一分子篩選,因而無法避免篩選失誤。
上述侷限,極大限制了DEL的成藥能力。因此,DEL技術被提出已近30年,真正應用於工業化也不過十幾年。
與其他技術相比,too young。
國內企業中,除了成都先導強調DEL技術之外,其他CRO企業一般也就是配備DEL的開發平臺供客戶選擇,但都沒有太強調這一塊。
成都先導董秘耿世偉曾表示,藥明康德和成都先導的業務定位、客戶群體和商業模式有較大差異,不存在重大影響。事實上,對於藥明康德來說,DEL只能算是閒棋冷子,還遠不到發揮決定作用的時候。
但新藥開發的格局可能真的會變化。
DEL技術的最大應用可能會在PROTAC領域,這是一種針對無法成藥靶點的技術,用類似貼上的方式,抓住不好被常用藥物“抓住”的靶蛋白,然後再集中消除。這樣,DEL技術開發出的千奇百怪的化學結構,就都能派上用場了。
不可成藥靶點佔到人類目前已知靶點的80%左右,如果PROTAC技術能夠帶著DEL組合出的化合物,攻克這些靶點,今後,人類能用到的特效藥還將成倍增加。
重點是,這些未來的“創新藥”,很有可能都是計算機算出來的。
AI來襲
如果將學習能力超強的AI,與高通量分析篩選技術DEL相結合呢?
2017年夏天,谷歌公司的AlphaGo只是學習了韓國圍棋大師李世石的棋譜,便打敗了2萬多盤圍棋經驗的柯潔。
2018年前後,中國湧現大量的AI製藥公司。對此,國內一家知名投資機構創始人表示:利用積累的資料和技術,AI有望輔助DEL儘快發揮作用。
就DEL技術本身而言,分子庫的建設及篩選方法才是關鍵。這兩點,AI剛好可以幫上忙。因此,DEL+AI已經成了AI製藥企業的標配,前者是技術路徑,後者為前者提升效率。
例如2018年成立的阿爾脈生物,已經開始用整合了AI的DEL平臺接單,吸引先聲藥業、再鼎醫藥與其簽訂新藥發現合作協議。
華為盤古云藥物分子大模型,並沒有明確是否與DEL相結合,但這一步一定是超前的。事實上2015年以來,各大網際網路巨頭都在投資AI製藥領域:
騰訊在2015年和2018年參與晶泰科技的 A 輪及 B 輪融資。2020年7月釋出了“雲深智藥”AI驅動藥物發現平臺;
阿里雲與全球健康藥物研發中心(GHDDI)合作,開發 AI 藥物研發和大資料平臺。GHDDI由清華大學、蓋茨基金會和北京市政府共同發起成立;
百度2020 年 9 月成立百圖生科進軍 AI 製藥領域;
位元組跳動2016年成立的AI Lab突然在2020年底宣佈,在北京、上海、美國三地的正式招聘 AI 製藥領域人才。
當有一天,成都先導、藥明康德們發現自己的對手不是CRO,而是網際網路巨頭時,AI製藥領域才會真正開始有趣。
目前,國內AI製藥公司的研究路徑各不相同,水平參差不齊。然而,泥沙俱下的環境中,也可能孕育新一代的生力軍。
文丨煙醯胺
運營|廿十三
每天兩篇深度稿件,解碼醫藥健康
#藥企AI+DEL##AI製藥##華為盤古#