2021年美國聖安東尼奧乳腺癌研討會(SABCS)即將於當地時間12月7日至10日以線上+線下相結合的方式召開。近日,2021 SABCS摘要內容正式公佈,多項重磅研究即將揭曉,讓我們一睹為快吧!
研究背景
HER2突變是轉移性乳腺癌(MBC)的一個重要致癌驅動因素。來那替尼(N)是一種口服、不可逆的泛HER型酪氨酸激酶抑制劑,具有抗HER2突變的臨床前和臨床活性。來那替尼±氟維司群(F)後配對活檢的基因組分析表明,對來那替尼的耐藥性可能透過突變等位基因的擴增或獲得繼發HER2突變發生。
在SUMMIT試驗中,HR+/HER2突變的MBC患者,包括既往接受過週期性蛋白依賴性激酶抑制劑(CDK4/6i)的患者[Jhaveri et al. SABCS 2020],在N+F中加入曲妥珠單抗(T)顯示出令人鼓舞的臨床活性。基於這些發現,為了更好地理解N對N+F+T組合活性的貢獻,SUMMIT研究最近已擴充套件到包括對暴露於CDK4/6i的HR+、HER2突變、HER2陰性MBC患者的N+F+T與F+T與F的隨機Simon 2期比較。階段1的註冊現在已經完成(N+F+T, n=7;F + T、n = 7;F, n=7),一旦資料成熟,就會得出結果。本文中,我們報告了SUMMIT試驗中乳腺癌佇列的最新發現,這些資料目前是可用的。
研究方法
2期SUMMIT試驗(NCT01953926)納入了HR+、HER2陰性的MBC患者,這些患者的腫瘤經基因組測序鑑定有啟用的HER2突變。在開始試驗的隨機部分之前,這些患者被納入非隨機佇列,並接受N+F+T(口服N 240mg/d,i.m. F 500mg第1週期d1&15,然後q4w,i.v. T 8mg/kg,然後6 mg/kg q3w)。在試驗的隨機部分開始後,這些患者接受N+F+T, F+T或F(1:1:1比例)。HER2突變三陰性乳腺癌(TNBC)患者被納入非隨機佇列並接受N+T治療。在前2個治療週期中,必須進行洛哌丁胺預防。對於MBC的系統治療種類沒有限制。療效終點:研究人員評估的客觀緩解率(ORR)和臨床獲益率(RECIST v1.1或其他定義標準);反應時間;最好的總體反應。
研究結果
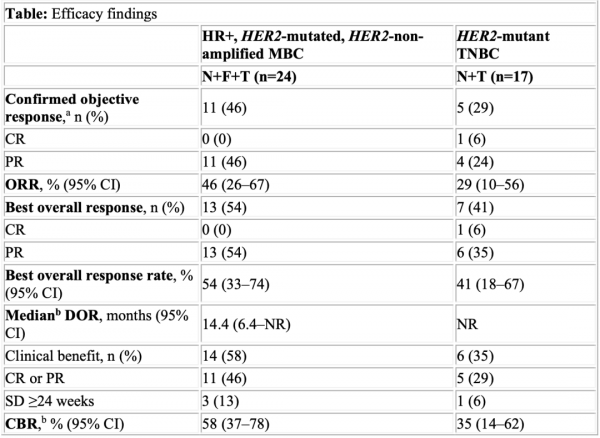
在納入隨機佇列之前,截止2021年6月18日,24例曾接受過CDK4/6i的HR+ HER2突變MBC患者被納入非隨機佇列並接受N+F+T, 17例HER2突變TNBC患者被納入並接受N+T。隨機化患者的資料還不成熟。兩組患者的HER2等位基因變異(患者可能有>1突變);激酶域熱點(n=26);exon-20插入(n = 9);細胞外區域熱點(n=4);exon-19刪除(n = 1);跨膜域錯義(n=1);激酶域非熱點(n=2)。療效結果見表。腹瀉是最常見的不良事件:N+F+T(非隨機佇列),96%;N+T(TNBC佇列)94%。無4級腹瀉報告。
N+F+T對於HR+HER2突變MBC且既往暴露於CDK4/6抑制劑的患者是一個很有前景的組合。在HER2突變的TNBC中,N+T也表現出令人鼓舞的活性。在HR+HER2突變MBC患者中隨機比較N+F+T與F+T與F的第一個結果(Simon 1期分析)將在會議上公佈。
參考文獻:
GS4-10 Neratinib + fulvestrant + trastuzumab for hormone receptor-positive, HER2-mutant metastatic breast cancer and neratinib + trastuzumab for triple-negative disease: Latest updates from the SUMMIT trial. 2021 SABCS