本文來自微信公眾號:X-MOLNews
提到芳香化合物的去芳構化(dearomatization),估計不少讀者立馬會想到Birch 還原反應。如圖1A所示,Birch 還原反應一般是在液氨中用鋰、鈉或鉀將芳烴去芳構化為1,4-環己二烯,儘管操作繁瑣且有不小的安全風險,但這一有半個世紀歷史的“老反應”在製藥業、香水業以及各個有機化學實驗室中都相當常見。長期以來,液氨被認為是Birch 還原反應所必不可少的溶劑,以溶解鹼金屬形成溶劑化電子。如果不用液氨而用其他更易操作和更安全的試劑,顯然會大大改進Birch還原反應,化學家們數十年來也陸續獲得一些進展,開發了一些無氨條件,例如:1)Benkeser 等人使用鋰和有機胺來還原芳烴化合物,但可能會得到過度還原產物的混合物(圖1B);2)Dolby等人則用鋰、有機胺與叔丁醇,但底物範圍有限;3)Donohoe等人在-78 ℃下用二叔丁基聯苯與鋰還原缺電子芳烴和雜環化合物(圖1C),但該過程對氧氣高度敏感;4)安傑等人利用鈉與15-冠-5實現了富電子或中性底物的還原(圖1D);5)Baran等人報道了富電子芳烴的電化學還原(圖1E)。以上方法,或多或少受制於底物範圍窄、操作複雜、裝置要求高、反應條件苛刻等諸多限制,因此,開發一種簡單、高效、快速、可規模化應用的Birch還原方法對於產業界及學術界來說都至關重要。
2004年,Sugai小組在四氫呋喃(THF)或Et2O中用鋰和乙二胺還原芳烴化合物時沒有分離出1,4-環己二烯產物,這表明THF可能是鋰離子的配體。受此啟發,美國匹茲堡大學的Kazunori Koide教授課題組在溫和條件下以四氫呋喃為溶劑,利用鋰和乙二胺促進了芳烴化合物的Birch還原反應(圖1F)。該方法在室溫下反應、裝置要求低、操作簡便、成本低、快速、可規模化、安全性高,而且對富電子和缺電子芳烴都有很好的效果,可稱得上是“在任何化學實驗室都適用”(注:這是論文中的原話,“accessible to any chemical laboratory”)。相關成果近日發表在Science 上。
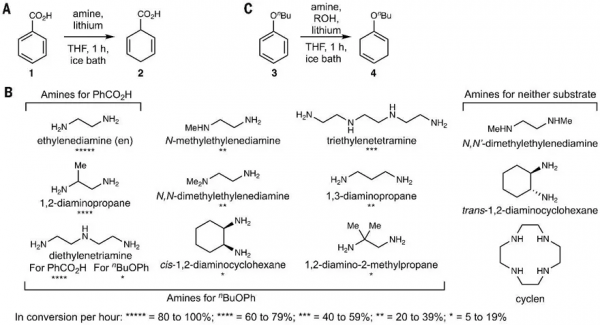
圖1. Birch還原反應型別。圖片來源:Science
首先,作者選擇苯甲酸1為模型底物,將一個充滿氨氣的氣球連線到含有鋰、底物1和THF的燒瓶上,以83%的收率獲得二烯產物 2(圖2A)。不過,該體系對於富電子芳烴的效果不佳,為此作者對不同結構和種類的胺配體進行了深入的研究(圖2B)。在苯甲酸體系下的研究表明:1)乙二胺(5.0 equiv)與鋰(2.5 equiv)二者缺一不可;2)大部分的胺配體均不反應;3)1,2-丙二胺、乙二胺以及二亞乙基三胺均可促進反應發生,考慮價格和活性的原因最終選擇乙二胺為最佳配體,特別是將反應規模放大到10 g時,也能以95%的分離收率獲得產物2。緊接著,作者以苯丁醚為模板底物對富電子芳烴的還原條件進行了探索(圖2C),實驗結果表明:1)在無醇的條件下,底物並不反應,這與前人報道的機制一樣;2)對不同的醇進行篩選後發現,叔丁醇的效果最好(主產物4的收率為75%,過度還原產物5的收率為11%);3)對胺配體的篩選發現,乙二胺同樣是最佳的選擇。為了充分消耗底物,作者將鋰和乙二胺的當量分別增加到 3 和 6,最終以 85% 的產率獲得二烯 4。
圖2. 條件篩選總結。圖片來源:Science
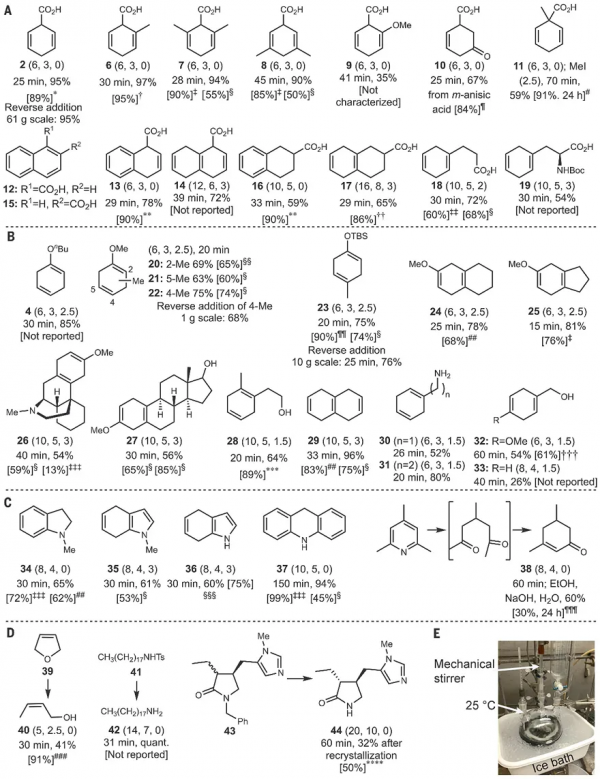
在最優條件下,作者對底物範圍進行了考察(圖3)。如圖3A所示,苯甲酸及其類似物均能以高產率得到相應的還原產物(2、6-10)。有趣的是,當用碘甲烷淬滅苯甲酸的還原反應時,得到了相應的烷基化產物11(產率59%)。此外,羧酸12在無/有叔丁醇的情況下得到典型的Birch還原產物13(產率78%)或三烯14(產率72%);而羧酸15則在無/有叔丁醇時被還原為酸16(產率59%)或二烯17(產率65%)。類似地,正丁基苯甲醚、2-、3-和4-甲基苯甲醚、6-甲氧基四氫化萘、苄胺和苯乙胺均能以中等至較好的收率獲得相應的二烯產物(4、20-22、24、30-31,圖3B),而萘則得到三烯產物29。儘管該方法與Baran小組先前報道的方法制備烷基烯醇矽醚23的產率相當,但是該反應的速率更快。值得一提的是,該反應對於藥物分子(如止咳藥右美沙芬26、雌酮-3-甲醚27)和合成中間體(25、28)同樣有效。其次,N-甲基吲哚在無/有叔丁醇的條件下能以中等的收率獲得產物34或35(圖3C)。吲哚和吖啶也能相容該反應,分別被還原為吡咯36和二氫吖啶37,特別是2,4,6-吡啶在無叔丁醇的條件下能以60%的產率得到環己烯酮38。最後,該反應還能實現2,5-二氫呋喃39的開環、磺醯胺41和內醯胺43的脫保護,從而分別得到Z-烯丙醇40、胺42和醯胺44(圖3D)。
圖3. 底物拓展。圖片來源:Science
作者進一步研究了該方法的規模化前景,結果表明:1)攪拌速率越快,反應進行得越快;2)當底物1或3的濃度增加至0.8 M時,也可以加快反應速率;3)透過改變加料方式並及時散熱,可以將反應放大至61 g規模(圖3E);4)將內部溫度控制在10-26 ℃,能以95%的收率獲得產物2。基於上述探索,作者大大縮短了4-甲基苯甲醚和4-OTBS-甲苯(10 g規模)還原為二烯22與23的反應時間。事實上,對於Birch還原反應而言,吸電子基團會提高還原速率,而給電子基團則會降低還原速率,例如傳統條件下苯甲酸酯的Birch還原速率是苯甲醚的61倍以上。如圖4A所示,將PhCO2H和nBuOPh的等摩爾混合物、乙二胺和鋰置於無醇的條件下進行反應,分別以59%和7%的產率獲得酸2和醚4。值得一提的是,當用三亞乙基四胺代替乙二胺並加入叔丁醇後,作者發現富電子芳烴nBuOPh要比缺電子芳烴PhCO2H反應性更高(酸2和醚4比例為1:2)。此外,作者將Birch還原與銅鹽化學相結合,以20%的收率獲得季碳產物45(圖4B),進一步證實了該方法並不會影響碳負離子中間體的反應性。
圖4. 選擇性以及反應性的調節。圖片來源:Science
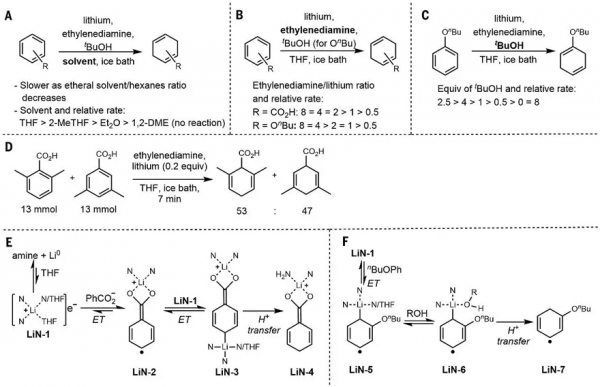
接著,作者研究了不同條件下nBuOPh和PhCO2H的還原動力學。研究表明:1)還原速率取決於THF的濃度以及醚類溶劑(圖5A),反應介質極性降低可能會影響氨穩定的自由基陰離子的穩定性和溶解度;2)乙二胺/鋰比值增加,反應速率也隨之增加(圖5B);3)當叔丁醇從0當量增加到2.5當量時,還原速率穩步增加(圖5C),而超過2.5當量後還原速率會顯著降低。在此基礎上,作者提出了苯甲酸Birch還原的反應機理(圖5E)。首先,Li(0)與胺配體在THF中配位溶解形成LiN-1,後者經電子轉移得到自由基陰離子LiN-2。接著,再發生電子轉移得到LiN-3,後者被質子化形成LiN-4。類似地,圖5F展示了nBuOPh的Birch還原機制,即電子從LiN-1轉移到底物上形成自由基陰離子LiN-5,隨後LiN-5與叔丁醇結合產生LiN-6,從而觸發分子內質子化反應得到自由基物種LiN-7。
圖5. 反應機理研究。圖片來源:Science
總結
Kazunori Koide教授課題組在四氫呋喃中利用鋰和乙二胺實現了苯甲酸的Birch還原反應,而醇的加入則實現了給電子芳烴的Birch還原,他們通過後期調控鋰、胺和醇的用量,有效地控制了底物的還原程度。透過鋰介導還原和脫保護來構建複雜分子的策略更容易被科學界所接受,並可以快速高效地構建多種活性中間體。最後,透過將有機鋰化學與其它有機金屬化學相結合,可進一步擴大Birch還原反應的範圍。
Scalable Birch reduction with lithium and ethylenediamine in tetrahydrofuran
James Burrows, Shogo Kamo, Kazunori Koide
Science, 2021, 374, 741-746, DOI:10.1126/science.abk3099
導師介紹
Kazunori Koide
https://www.x-mol.com/university/faculty/1728
(本文由吡哆醛供稿)