近日,南開大學醫學院嶽世靜副教授聯合南開大學化學學院肖樂輝教授課題組在國際著名學術期刊J Extracell Vesicles發表了研究論文。其研究首次證明了TSPAN8分子可以促進sEVs與受體細胞的限制性擴散,進而提高靶細胞的攝取並促進腫瘤細胞的遷移和EMT並誘導腫瘤轉移。
近年來,sEVs由於其特異優勢而被廣泛的應用於疾病的診斷與治療。sEVs包裝大量的生物活性分子可以透過血流輸送至機體多種器官組織。sEVs在細胞間通訊中具有關鍵調節作用,sEVs裝載大量生物活性分子可能會影響受體細胞的表型和功能。有研究表明sEVs荷載分子可以調控生理或病理微環境靶細胞的表型。上皮樣癌細胞來源的sEVs富集CD151或TSPAN8與整合素Integrins分子相互作用形成複合物,可促進腫瘤進展。然而,有關sEVs與受體細胞的結合過程及相關分子調節機制還不明確。
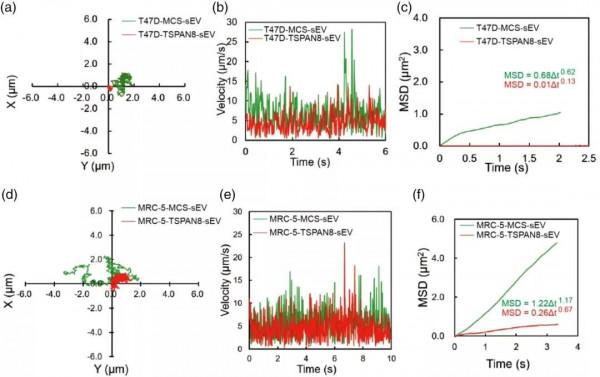
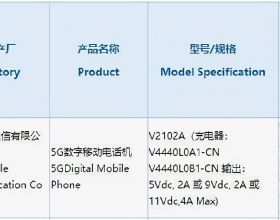
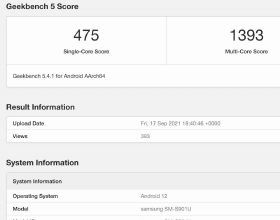
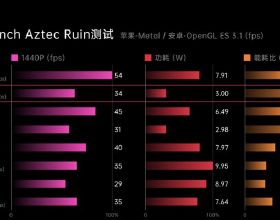
研究團隊透過基因工程手段調節乳腺癌細胞表達四次跨膜蛋白8(Tetraspanin 8, TSPAN8),透過表達TSPAN8乳腺癌細胞來源的微小細胞外囊泡(small extracellular vesicles, sEVs)與靶細胞的相互作用,研究TSPAN8分子對sEVs在靶細胞膜表面的擴散和轉運特性的影響。
此外,研究團隊運用單粒子追蹤技術證明TSPAN8分子透過對sEVs的限制性擴散顯著促進與受體細胞的結合。進一步功能分析表明,表達TSPAN8的sEVs顯著促進了癌細胞的運動性和上皮間充質樣轉化(epithelial-mesenchymal transition, EMT)。該研究有利於明確TSPAN8分子修飾sEVs為藥物遞送系統應用提高效率。
同時,體內研究表明,表達TSPAN8的sEVs顯著促進了肝臟、肺和脾臟中的結合和滯留。該研究表明TSPAN8透過加強限制性擴散促進sEVs與靶細胞間的相互作用,並顯著促進細胞的運動。因此,表達TSPAN8的sEVs可作為重要的直接或間接腫瘤治療靶點。
本文第一作者為南開大學醫學院碩士研究生王騰、南開大學化學學院博士研究生王鑫和成都第三人民醫院的王浩斌副主任醫師。醫學院碩士研究生李路瀚和張陳紅深度參與了該研究。南開大學化學學院肖樂輝教授和南開大學醫學院嶽世靜副教授為共同通訊作者,南開大學為第一完成單位。該研究得到了國家自然科學基金委的專案資助。
延伸閱讀:
嶽世靜,南開大學醫學院副教授。研究方向(包括承擔課題專案):腫瘤發生發展;腫瘤診斷治療;細胞外囊泡功能與轉化。他曾獲國際胞外囊泡學會年會最佳學術報告獎(2017.5.22,加拿大,多倫多,國際胞外囊泡學會)。
肖樂輝,博士,特聘研究員。研究領域:高靈敏單分子檢測分析;功能奈米材料的製備其生物顯微成像分析;奈米顆粒光學效能調控顯微成像研究。
更多精彩資訊,歡迎關注"南開大學本科招生"頭條號
本文素材來自:南開大學醫學院、南開大學化學學院等